Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
1) этилен
2) ацетилен
3) этан
4) пропилен
22. С помощью бромной воды можно различить
1) пропан и этан
2) пропин и этин
3) ацетилен и дивинил
4) пропин и пропан
23. Бензол и стирол можно распознать
1) раствором NaOH
2) нитрующей смесью
3) раствором AgNO 3
4) раствором КMnO 4
24. Установите соответствие между формулой углеводорода и его названием.
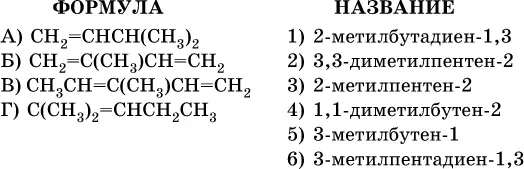
25. Процесс, не относящийся к переработке нефти, – это
1) перегонка
2) крекинг
3) риформинг
4) коксование
26. При крекинге нефти из октана образуются
1) бутан
2) этан
3) этилен
4) бутилен
27. Продукт полимеризации этилена (полиэтилен) отвечает формуле
1) (СН 2) n(—СН=СН—) n
3) (—СН 2—СН 2—) n
4) (СН 2=СН 2) n
28. Для промышленного синтеза бутадиенового каучука используют мономер
1) CH 2=CHCH=CH 2
2) CH 2 =CH—C≡CH
3) CH 3CH=C=CH 2
4) CH 2=C(CH 3)C≡CH
29. Мономер пластмассы тефлон (политетрафторэтилен) синтезируют по реакции
1) замещения СCl 2+ F 2 →…
2) пиролиза CHClF 2
3) окисления CCl 2F 2
4) фторирования С 2Н 6
10. Кислородсодержащие органические соединения
10.1. Спирты. Простые эфиры. Фенолы
Спирты– производные углеводородов, содержащие функциональную группу ОН(гидроксил). Спирты, в которых имеется одна группа ОН, называются одноатомными, а спирты с несколькими группами ОН — многоатомными.
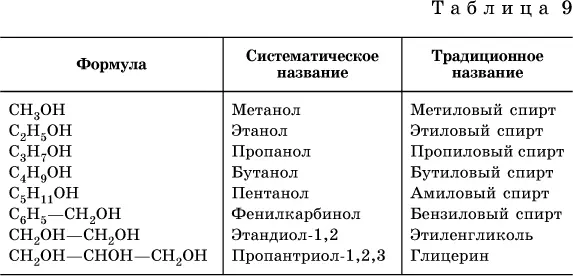
Названия некоторых распространенных спиртов приведены в табл. 9.
По строению различают спирты первичные, вторичные и третичные, в зависимости от того, при каком атоме углерода (первичном, вторичном или третичном) находится группа ОН:
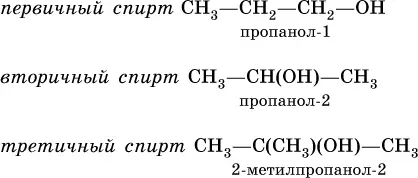
Одноатомные спирты – бесцветные жидкости (до Cl 2Н 25ОН), растворимые в воде. Простейший спирт — метанол СН 3ОН чрезвычайно ядовит. С увеличением молярной массы температура кипения спиртов повышается.
Молекулы жидких одноатомных спиртов ROH ассоциированы за счет водородных связей:
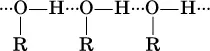
(эти связи аналогичны водородным связям в чистой воде).
При растворении в воде молекулы ROH образуют водородные связи с молекулами воды:
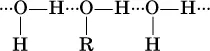
Водные растворы спиртов ROH имеют нейтральную среду; другими словами, спирты практически не диссоциируют в водном растворе ни по кислотному, ни по основному типу.
Химические свойства одноатомных спиртов обусловлены присутствием в них функциональной группы ОН.
Водород группы ОН в спиртах может замещаться на металл:
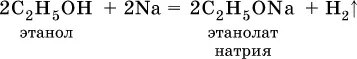
Этанолаты и производные других спиртов (алкоголяты) легко гидролизуются:
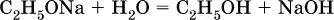
Группу ОН в спиртах можно заместить на Cl или Br:
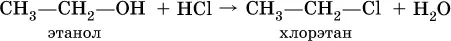
При действии на спирты водоотнимающих средств, например концентрированной H 2SO 4, происходит межмолекулярная дегидратация:
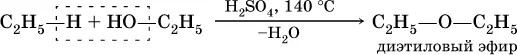
Продукт реакции — диэтиловый эфир (С 2Н 5) 2O – относится к классу простых эфиров.
В более жестких условиях дегидратация становится внутримолекулярной и образуется соответствующий алкен:
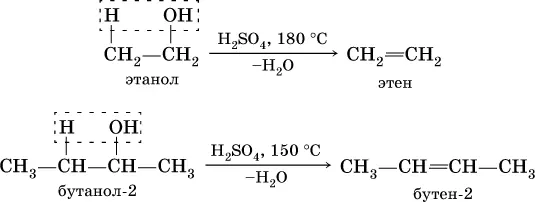
Многоатомные спирты рассмотрим на примере простейших представителей двух– и трехатомных спиртов:
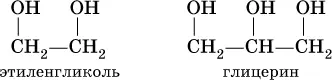
При комнатной температуре они – бесцветные вязкие жидкости с температурами кипения 198 и 290 °C соответственно, неограниченно смешиваются с водой. Этиленгликоль ядовит.
Химические свойства многоатомных спиртов подобны свойствам спиртов ROH. Так, в этиленгликоле одну или две группы ОН можно заместить на галоген:
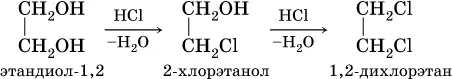
Кислотные свойства многоатомных спиртов проявляются в том, что (в отличие от одноатомных спиртов) водород группы ОН замещается на металл под действием не только металлов, но и гидроксидов металлов:
а)
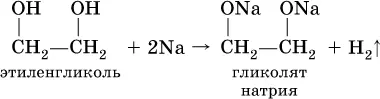
б)
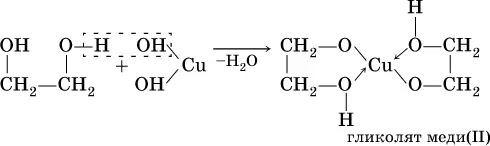
(стрелками в формуле гликолята меди показано образование ковалентных связей медь – кислород по донорно-акцепторному механизму).
Аналогично реагирует с гидроксидом меди (II) глицерин:
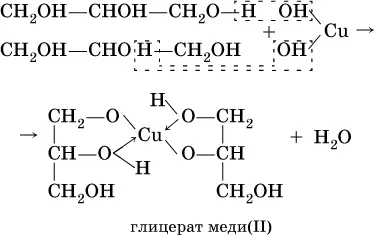
Гликолят и глицерат меди (II), имеющие ярко-синюю окраску, позволяют качественно обнаруживатьмногоатомные спирты.
Получение одноатомных спиртов в промышленности– гидратация алкенов в присутствии катализаторов (H 2SO 4, Al 2O 3), причем присоединение воды к несимметричным алкенам происходит по правилу Марковникова:
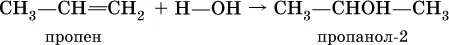
(способ получения вторичного спирта), или присоединение к алкенам СО и Н 2в присутствии кобальтового катализатора (процесс называется гидрофоржилирование):
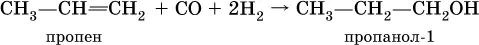
(способ получения первичного спирта).
В лаборатории(а иногда и в промышленности) спирты получают взаимодействием галогенпроизводных углеводородов с водой или водным раствором щелочи при нагревании:
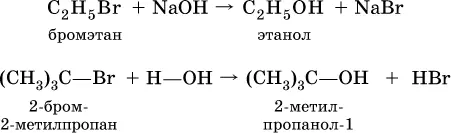
Этанол С 2Н 5ОН образуется также при спиртовом брожении сахаристых веществ, например глюкозы:
Читать дальшеИнтервал:
Закладка:










