Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
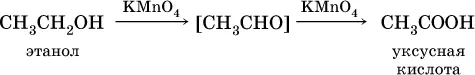
Более подходящим окислителем является оксид меди (II):
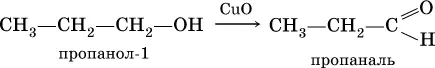
Ацетальдегид в промышленностиполучают по реакции Кучерова (см. 19.3).
Наибольшее применение из альдегидов имеют метаналь и этаналь. Метаналь используют для производства пластмасс (фенопластов), взрывчатых веществ, лаков, красок, лекарств. Этаналь – важнейший полупродукт при синтезе уксусной кислоты и бутадиена (производство синтетического каучука). Простейший кетон – ацетон используют в качестве растворителя различных лаков, ацетатов целлюлозы, в производстве кинофотопленки и взрывчатых веществ.
10.3. Карбоновые кислоты. Сложные эфиры. Жиры
Карбоновые кислоты – это производные углеводородов, содержащие функциональную группу СООН ( карбоксил).
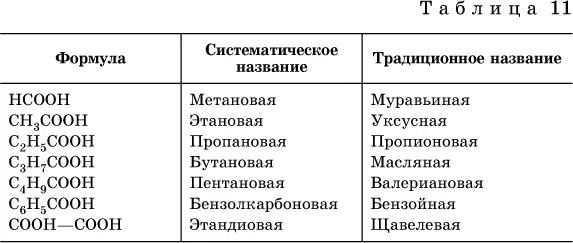
Формулы и названия некоторых распространенных карбоновых кислот приведены в табл. 11.
Традиционные названия кислот НСООН ( муравьиная), СН 3СООН (уксусная), С 6Н 5СООН (бензойная) и (СООН) 2 (щавелевая) рекомендуется использовать вместо их систематических названий.
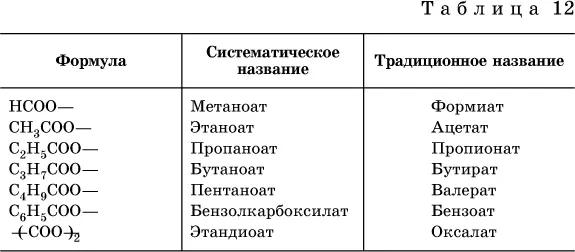
Формулы и названия кислотных остатков приведены в табл. 12.
Для составления названий солей этих карбоновых кислот (а также их сложных эфиров, см. ниже) обычно используются традиционные названия, например:

Низшие карбоновые кислоты – бесцветные жидкости с резким запахом. При увеличении молярной массы температура кипения возрастает.
Карбоновые кислоты обнаружены в природе:

Простейшие карбоновые кислоты растворимы в воде, обратимо диссоциируют в водном растворе с образованием катионов водорода:
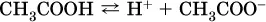
и проявляют общие свойства кислот:
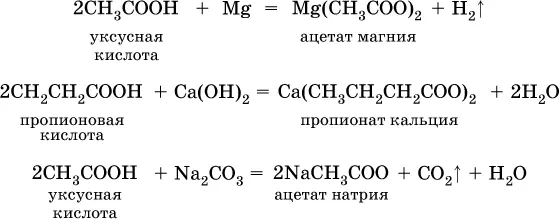
Важное практическое значение имеет взаимодействие карбоновых кислот со спиртами (подробнее см. ниже):
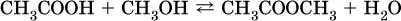
Отметим, что кислота НСООН вступает в реакцию «серебряного зеркала» как альдегиды:
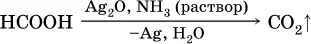
и разлагается под действием водоотнимающих реактивов:
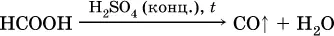
Получение:
• окисление альдегидов:
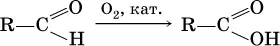
• окисление углеводородов:
а)
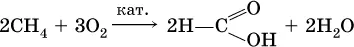
б)
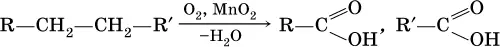
Кроме того, муравьиную кислоту получают по схеме:
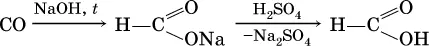
а уксусную кислоту – по реакции:
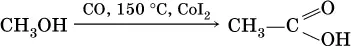
Применяют муравьиную кислоту как протраву при крашении шерсти, консервант фруктовых соков, отбеливатель, дезинфекционный препарат. Уксусную кислоту используют как сырье в промышленном синтезе красителей, медикаментов, ацетатного волокна, негорючей кинопленки, органического стекла. Натриевые и калиевые соли высших карбоновых кислот – основные компоненты мыла.
Сложные эфиры– продукты обменного взаимодействия карбоновых кислот со спиртами. Это взаимодействие называется реакцией этерификации:
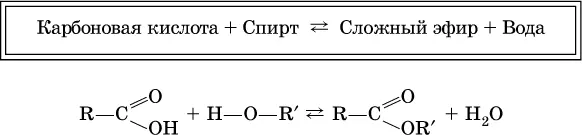
Механизм реакции этерификации был установлен при использовании спирта, меченного изотопом 18O; этот кислород после реакции оказался в составе эфира(а не воды):
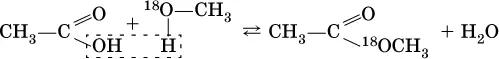
Следовательно, в отличие от реакции нейтрализации неорганической кислоты щелочью (Н ++ ОН -= Н 2O), в реакции этерификации карбоновая кислота всегда отдает группу ОН, спирт – атом Н(образуется вода). Реакция этерификации обратима; она лучше протекает в кислотнойсреде, обратная реакция ( гидролиз, омыление) – в щелочной среде.
Формулы и названия распространенных сложных эфиров приведены в табл. 13.
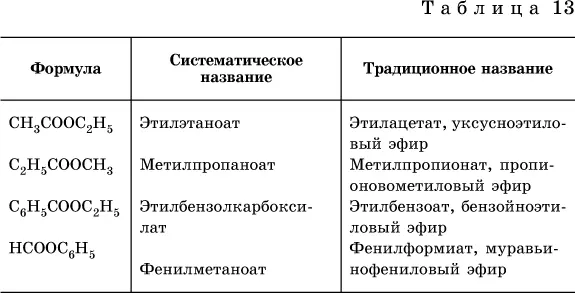
Среди сложных эфиров есть бесцветные низкокипящие горючие жидкости с фруктовым запахом, например:
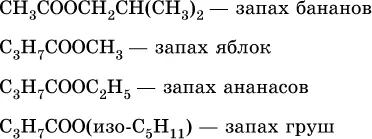
Используются сложные эфиры как растворители для лаков, красок и нитратов целлюлозы, носители фруктовых ароматов в пищевой промышленности.
Сложные эфиры трехатомного спирта – глицерина и высших карбоновых кислот (в общем виде RCOOH), например с формулами и названиями:
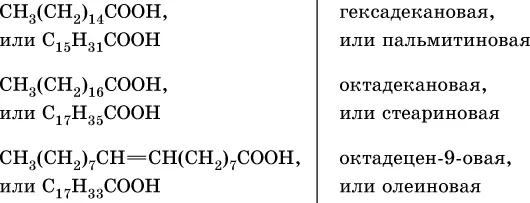
носят названия жиров. Примером жира будет смешанный сложный эфир глицерина и этих кислот:
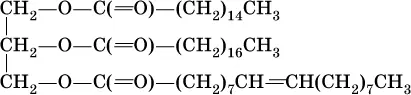
Чем выше содержание остатков олеиновой кислоты (или других ненасыщенных кислот), тем ниже температура плавления жира. Жидкие при комнатной температуре жиры называются маслами. Путем гидрогенизации, т. е. присоединения водорода по двойной связи, масла превращают в твердые жиры (например, растительное масло – в маргарин). Реакция этерификации (образования жира) обратима:
Читать дальшеИнтервал:
Закладка:










