Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
- 180 -
Нарушение равновесия вследствие изменения давления (путем уменьшения или увеличения объема системы). Когда в реакции участвуют газы, равновесие может нарушиться при изменении объема системы.
Рассмотрим влияние давления на реакцию между монооксидом азота и кислородом:
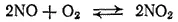
Пусть смесь газов NO, O 2и NO 2находится в химическом равновесии при определенной температуре и давлении. Не изменяя температуры, увеличим давление так, чтобы объем системы уменьшился в 2 раза. В первый момент парциальные давления и концентрации всех газов возрастут вдвое, но при этом изменится соотношение между скоростями прямой и обратной реакций — равновесие нарушится.
В самом деле, до увеличения давления концентрации газов имели равновесные значения [NO] равн, [O 2] равни [NO 2] равн, а скорости прямой и обратной реакций были одинаковы и определялись уравнениями:
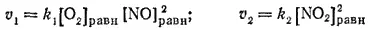
В первый момент после сжатия концентрации газов увеличатся вдвое по сравнению с их исходными значениями и будут равны соответственно 2[NO] равн, 2[O 2] равни 2[NO 2] равн. При этом скорости прямой и обратной реакций будут определяться уравнениями:
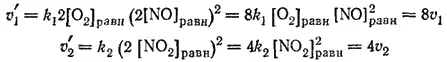
Таким образом, в результате увеличения давления скорость прямой реакции возросла в 8 раз, а обратной — только в 4 раза. Равновесие в системе нарушится — прямая реакция будет преобладать над обратной. После того как скорости сравняются, вновь установится равновесие, но количество NO 2в системе возрастет, равновесие сместится вправо.
Нетрудно видеть, что неодинаковое изменение скоростей прямой и обратной реакций связано с тем, что в левой и в правой частях уравнения рассматриваемой реакции различно число молекул газов: одна молекула кислорода и две молекулы монооксида азота (всего три молекулы газов) превращаются в две молекулы газа — диоксида азота. Давление газа есть результат ударов его молекул о стенки сосуда; при прочих равных условиях давление газа тем выше, чем больше молекул заключено в данном объеме газа. Поэтому реакция, протекающая с увеличением числа молекул газов, приводит к возрастанию давления, а реакция, протекающая с уменьшением числа молекул газов, — к его понижению.
Помня об этом, вывод о влиянии давления на химическое равновесие можно сформулировать так:
При увеличении давления путем сжатия системы равновесие сдвигается в сторону уменьшения числа молекул газов, т. е. в сторону понижения давления, при уменьшении давления равновесие сдвигается в сторону возрастания числа молекул газов, т. е. в сторону увеличения давления.
В том случае, когда реакция протекает без изменения числа молекул газов, равновесие не нарушается при сжатии или при расширении системы. Например, в системе
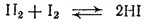
равновесие не нарушается при изменении объема; выход HI не зависит от давления.
Нарушение равновесия вследствие изменения температуры. Равновесие подавляющего большинства химических реакций сдвигается при изменении температуры. Фактором, который определяет направление смещения равновесия, является при этом знак теплового эффекта реакции. Можно показать, что при повышении температуры равновесие смещается в направлении эндотермической, а при понижении — в направлении экзотермической реакции.
Так, синтез аммиака представляет собой экзотермическую реакцию
N 2+ 3H 2= 2NH 3+ 92,4 кДж
Поэтому при повышении температуры равновесие в системе H 2- N 2- NH 3сдвигается влево — в сторону разложения аммиака, так как этот процесс идет с поглощением теплоты.
Наоборот, синтез оксида азота (II) представляет собой эндотермическую реакцию:
N 2+ O 2= 2NO - 180,5 кДж
Поэтому при повышении температуры равновесие в системе N 2- O 2- NO сдвигается вправо — в сторону образования NO.
Закономерности, которые проявляются в рассмотренных примерах нарушения химического равновесия, представляют собою частные случаи общего принципа, определяющего влияние различных факторов на равновесные системы. Этот принцип, известный под названием принципа Ле Шателье, в применении к химическим равновесиям можно сформулировать так:
Если на систему, находящуюся в равновесии, оказать какое-либо воздействие, то в результате протекающих в ней процессов равновесие сместится в таком направлении, что оказанное воздействие уменьшится.
Действительно, при введении в систему одного из веществ, участвующих в реакции, равновесие смещается в сторону расхода этого вещества. "При повышении давления оно смещается так, что давление в системе снижается; при повышении температуры равновесие смещается в сторону эндотермической реакции — температура в системе падает.
Принцип Ле Шателье распространяется не только на химические, но и на различные физико-химические равновесия. Смещение равновесия при изменении условий таких процессов, как кипение, кристаллизация, растворение, происходит в соответствии с принципом Ле Шателье.
65. Факторы, определяющие направление протекания химических реакций.
В предыдущих параграфах мы рассмотрели несколько примеров, показывающих, что при определенных условиях каждая химическая реакция самопроизвольно протекает в определенном направлении. Так, при низких температурах экзотермическая реакция образования парообразной воды
2H 2+ O 2= 2H 2O + 486,6 кДж
практически нацело протекает в прямом направлении*. Но при высоких температурах эта реакция начинает идти в обратном направлении: водяной пар разлагается на водород и кислород. Во всех случаях в результате реакции может быть достигнуто состояние устойчивого химического равновесия, но само положение равновесия при разных условиях оказывается различным.
Возникает вопрос; в чем причина определенной направленности химических процессов, какие факторы обусловливают то или иное состояние химического равновесия?
Известно, что в механических системах устойчивое равновесие соответствует минимуму потенциальной энергии системы. Так, шарик самопроизвольно скатывается из положения а на наклонной поверхности (рис. 69), причем его потенциальная энергия переходит сначала в кинетическую энергию движения шарика как целого, а затем в энергию теплового движения молекул. В положении б шарик находится в равновесии.
Естественно предположить, что и химические процессы должны самопроизвольно протекать в направлении уменьшения внутренней энергии системы, т. е. в направлении, отвечающем положительному тепловому эффекту реакции. Действительно, опыт показывает, что при обычных условиях самопроизвольно протекают преимущественно экзотермические реакции.
Читать дальшеИнтервал:
Закладка:






