Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир
- Название:Абсолютный минимум. Как квантовая теория объясняет наш мир
- Автор:
- Жанр:
- Издательство:Питер
- Год:2015
- Город:Санкт-Петербург
- ISBN:978-5-496-01069-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир краткое содержание
Физика — это сложнейшая, комплексная наука, она насколько сложна, настолько и увлекательна. Если отбросить математическую составляющую, физика сразу становится доступной любому человеку, обладающему любопытством и воображением. Мы легко поймём концепцию теории гравитации, обойдясь без сложных математических уравнений. Поэтому всем, кто задумывается о том, что делает ягоды черники синими, а клубники — красными; кто сомневается, что звук распространяется в виде волн; кто интересуется, почему поведение света так отличается от любого другого явления во Вселенной, нужно понять, что всё дело — в квантовой физике. Эта книга представляет (и демистифицирует) для обычных людей волшебный мир квантовой науки, как ни одна другая книга. Она рассказывает о базовых научных понятиях, от световых частиц до состояний материи и причинах негативного влияния парниковых газов, раскрывая каждую тему без использования специфической научной терминологии — примерами из обычной повседневной жизни. Безусловно, книга по квантовой физике не может обойтись без минимального набора формул и уравнений, но это необходимый минимум, понятный большинству читателей. По мнению автора, книга, популяризирующая науку, должна быть доступной, но не опускаться до уровня читателя, а поднимать и развивать его интеллект и общий культурный уровень. Написанная в лучших традициях Стивена Хокинга и Льюиса Томаса, книга популяризирует увлекательные открытия из области квантовой физики и химии, сочетая представления и суждения современных учёных с яркими и наглядными примерами из повседневной жизни.
Абсолютный минимум. Как квантовая теория объясняет наш мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Кривая потенциальной энергии, изображённая на рис. 12.1, получена на основе реальных квантовомеханических расчётов. Это относительно несложные вычисления, которые можно целиком выполнить с помощью карандаша и бумаги, компьютеры для этого не нужны. По результатам приближённых вычислений r 0=0,80 Å, так что они не вполне точны. Если хотите увидеть огромный объём математических выкладок, которые требуются даже для этого относительно простого расчёта, загляните в главу 17 моего учебника основ квантовой механики (Michael D. Fayer. Elements of Quantum Mechanics . New York: Oxford University Press, 2001). Намного более сложные квантовые теоретические вычисления для молекулы H 2позволяют получить все свойства молекулы водорода с точностью выше достижимой в экспериментальных измерениях. Точные вычисления возможны благодаря тому, что молекула водорода очень проста. Для крупных молекул эксперименты всё ещё превосходят вычисления по точности.
Образование связывающих молекулярных орбиталей
Из рис. 12.1 видно, что между двумя атомами водорода будет формироваться химическая связь, в результате чего образуются молекулы H 2, но неясно, каким образом. Как отмечалось в главе 11, ковалентная связь состоит в том, что атомы совместно используют электроны. Когда образуется молекула, атомные орбитали объединяются и формируют молекулярные орбитали. Для молекулы водорода мы начнём с двух атомов водорода: H a и H b . Каждый из них имеет один электрон атомной 1 s -орбитали. Обозначим эти орбитали 1 s a и 1 s b . В верхней части рис. 12.2 они показаны кружками. Это простое схематическое изображение делокализованной волны амплитуды вероятности электрона, представленной на рис. 10.2-10.4. В нижней части рисунка показано, что происходит, когда два атома сближаются так, что расстояние между ними становится равным длине химической связи r 0(см. рис. 12.1). Волновые функции имеют знак. В данном случае их знаки положительные.
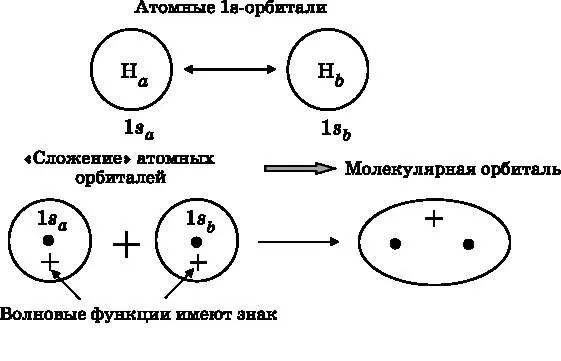
Рис. 12.2. Вверху схематически изображены две 1s-орбитали атомов водорода. В действительности это делокализованные волны амплитуды вероятности электронов, изображённые здесь в виде окружностей. В нижней части рисунка показано, что происходит, когда два атома сближаются и образуют молекулу H 2 . Две атомные орбитали объединяются и образуют молекулярную орбиталь
Волны амплитуды вероятности складываются и образуют молекулярную орбиталь. Мы довольно подробно обсуждали волны в главах 3 и 5. В главе 3 мы узнали, что волны при объединении могут давать конструктивную и деструктивную интерференцию. В главе 5 интерференция фотонов объяснялась через борновскую интерпретацию волновой функции как волны амплитуды вероятности. Теперь две волны амплитуды вероятности электрона, представляющие собой атомные орбитали, объединяются и в результате конструктивной интерференции образуют молекулярную орбиталь. Молекулярная орбиталь — это волна амплитуды вероятности. Возведённое в квадрат её абсолютное значение даёт вероятность обнаружения электронов в определённой области пространства.
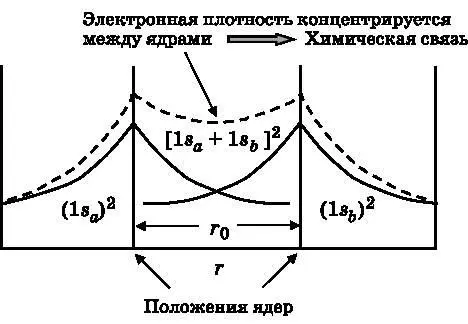
Рис. 12.3. Одномерный график квадратов двух 1s-орбиталей, принадлежащих атомам водорода: aи b(сплошные кривые), и квадрата суммы атомных орбиталей, который является квадратом молекулярной орбитали. Электронная плотность концентрируется между двумя ядрами
На рис. 12.3 представлен одномерный график распределения вероятности (квадрата волновой функции) для двух атомных орбиталей (1 s a и 1 s b ) и квадрат суммы атомных орбиталей. В центре атомных орбиталей находятся ядра атомов H, которые разделены расстоянием, равным длине химической связи r 0. Протоны (ядра) заряжены положительно и отталкиваются друг от друга. Однако молекулярная орбиталь концентрирует между ядрами электронную плотность, несущую отрицательный заряд, и тем удерживает их вместе. Важная особенность молекулярной орбитали состоит в том, что электроны больше не принадлежат одному или другому атому. Молекулярная орбиталь описывает делокализованное распределение вероятностей для двух электронов. Оба электрона свободно перемещаются по всей молекуле. Электроны, принадлежавшие разным атомам, когда те находились далеко друг от друга, теперь принадлежат всей молекуле. Они совместно используются атомами, которые больше не являются независимыми.
Связывающие и разрыхляющие молекулярные орбитали
До сих пор за рамками нашего обсуждения оставался один очень важный вопрос. Принцип Паули (см. главу 11) утверждает, что на любой орбитали может находиться максимум два электрона. Для образования молекулы водорода мы начинаем с двух атомов водорода. Каждый такой атом имеет 1 s -орбиталь. Согласно принципу Паули, на эти две орбитали можно поместить четыре электрона. У двух атомов водорода имеется только два электрона, но принцип Паули не нарушился бы, если бы на каждую атомную 1 s -орбиталь добавили ещё по одному электрону. Мы сложили две 1 s -орбитали и за счёт конструктивной интерференции получили одну молекулярную орбиталь. Принцип Паули гласит, что на эту молекулярную орбиталь можно поместить максимум два электрона. Мы начали с двух атомных орбиталей, которые содержат четыре электрона, но теперь у нас одна молекулярная орбиталь, которая может содержать два электрона. Чего-то явно не хватает. При образовании молекул места для электронов (орбитали) никогда не исчезают и не появляются. Если было две атомные орбитали, то должны образоваться две молекулярные орбитали, способные содержать четыре электрона.
На рис. 12.2 и 12.3 две атомные 1 s -орбитали водорода складывались с одинаковым знаком и давали молекулярную орбиталь, которая концентрирует электронную плотность между двумя атомными ядрами. Эти 1 s -орбитали являются волнами амплитуды вероятности и могут также складываться с противоположными знаками. При таком сложении атомные орбитали интерферируют деструктивно. Сложение с противоположными знаками изображено на рис. 12.4. Поскольку знаки двух атомных орбиталей противоположны, должно быть место, где положительная волна в точности гасит отрицательную волну. Это узел, подобный тем, что мы ранее обсуждали для волновой функции частицы в ящике и атомных орбиталей. Как видно из схемы на рис. 12.4, деструктивная интерференция между атомными орбиталями и получающиеся в результате узлы выталкивают электронную плотность из пространства между атомными ядрами. Отрицательно заряженные электроны больше не экранируют положительно заряженные ядра, которые отталкиваются. В отличие от кривой, полученной для сближения двух атомов водорода (см. рис. 12.1), в этом случае энергия не уменьшается, а возрастает.
Читать дальшеИнтервал:
Закладка:










