Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир
- Название:Абсолютный минимум. Как квантовая теория объясняет наш мир
- Автор:
- Жанр:
- Издательство:Питер
- Год:2015
- Город:Санкт-Петербург
- ISBN:978-5-496-01069-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Майкл Файер - Абсолютный минимум. Как квантовая теория объясняет наш мир краткое содержание
Физика — это сложнейшая, комплексная наука, она насколько сложна, настолько и увлекательна. Если отбросить математическую составляющую, физика сразу становится доступной любому человеку, обладающему любопытством и воображением. Мы легко поймём концепцию теории гравитации, обойдясь без сложных математических уравнений. Поэтому всем, кто задумывается о том, что делает ягоды черники синими, а клубники — красными; кто сомневается, что звук распространяется в виде волн; кто интересуется, почему поведение света так отличается от любого другого явления во Вселенной, нужно понять, что всё дело — в квантовой физике. Эта книга представляет (и демистифицирует) для обычных людей волшебный мир квантовой науки, как ни одна другая книга. Она рассказывает о базовых научных понятиях, от световых частиц до состояний материи и причинах негативного влияния парниковых газов, раскрывая каждую тему без использования специфической научной терминологии — примерами из обычной повседневной жизни. Безусловно, книга по квантовой физике не может обойтись без минимального набора формул и уравнений, но это необходимый минимум, понятный большинству читателей. По мнению автора, книга, популяризирующая науку, должна быть доступной, но не опускаться до уровня читателя, а поднимать и развивать его интеллект и общий культурный уровень. Написанная в лучших традициях Стивена Хокинга и Льюиса Томаса, книга популяризирует увлекательные открытия из области квантовой физики и химии, сочетая представления и суждения современных учёных с яркими и наглядными примерами из повседневной жизни.
Абсолютный минимум. Как квантовая теория объясняет наш мир - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
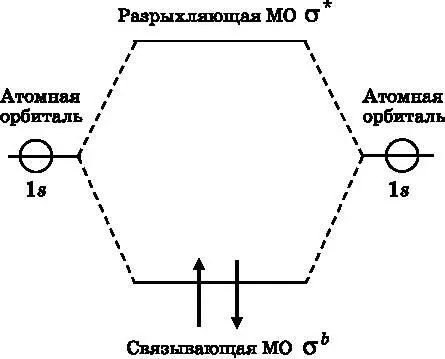
Рис. 12.7. Диаграмма МО молекулы водорода. Два электрона (стрелки), по одному от каждого атома водорода, занимают низший энергетический уровень, а их спины спарены. Их энергия ниже, чем у отдельных атомов. Тем самым за счёт совместного использования электронов образуется связь
Почему не существует молекулы гелия He 2? У каждого из двух отдельных атомов He на 1 s -орбитали имеется по два электрона. Поэтому диаграмма МО будет такой же, как на рис. 12.6. Однако теперь нам необходимо расселить по энергетическим уровням МО четыре электрона. На рис. 12.8 представлена диаграмма МО с четырьмя электронами. Первый электрон заселяется на связывающую МО, поскольку это низшее энергетическое состояние. Второй электрон также попадает на связывающую МО со спином, противоположным первому. Принцип Паули гласит, что ни у каких двух электронов не могут совпадать все квантовые числа. Два электрона на связывающей МО имеют разные спиновые квантовые числа: s =+½ и s =−½. Существуют только эти два значения спинового квантового числа, так что третий электрон не может попасть на связывающую МО. Он должен занять следующий энергетический уровень, который представлен разрыхляющей МО. Четвёртый электрон также может заселиться на разрыхляющую МО с противоположным спином. Два электрона на связывающей МО имеют энергию ниже, чем в отдельных атомах, но два электрона на разрыхляющей МО повышают энергию ровно настолько, насколько связывающие электроны её понижают. В результате не возникает никакого уменьшения энергии в сравнении с отдельными атомами. Целостность молекулы обеспечивается тем, что связанные атомы имеют более низкую энергию, чем отдельные атомы. В случае атомов гелия уменьшения энергии, которое привело бы к образованию устойчивой конфигурации, не происходит, и поэтому связь не возникает. В следующей главе мы познакомимся с аналогичным поведением благородного газа неона.
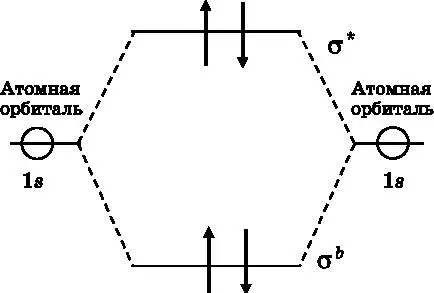
Рис. 12.8. Диаграмма МО гипотетической молекулы гелия. Имеется четыре электрона (стрелки), по два от каждого атома гелия. Два из них занимают связывающую МО. Два других в силу принципа Паули отправляются на разрыхляющую МО. В целом уменьшения энергии не происходит, и поэтому связь не возникает
Чтобы оценить прогностические возможности простых диаграмм, таких как изображённые на рис. 12.7 и 12.8, рассмотрим четыре возможные молекулы. Это молекулярный ион водорода H 2 +, молекула водорода H 2, молекулярный ион гелия He 2 +и молекула He 2. Молекулярный ион H 2 +состоит из двух ядер водорода (протонов) и одного электрона. Подобно одноатомному катиону Na +, он является положительно заряженным, поскольку электронов у него на один меньше, чем протонов. He 2 +— это молекулярный ион, состоящий из двух ядер гелия (по два протона в каждом) и трёх электронов. Таким образом, в нём имеется четыре положительно заряженных частицы (четыре протона) и три отрицательно заряженных электрона.
На рис. 12.9 представлена диаграмма энергетических уровней МО для этих четырёх молекул. Атомные энергетические уровни опущены. Молекулярный ион H 2 +имеет только один электрон, так что он занимает самый нижний энергетический уровень — связывающую МО. Энергия получается ниже, чем у разделённых атомов, но лишь на величину, примерно вдвое меньшую, чем у молекулы H 2, которая имеет два электрона на связывающей МО. Молекула H 2обладает полной ковалентной связью. Говорят, что она имеет порядок связи, равный 1. Молекулярный ион H 2 +имеет порядок связи, равный ½.
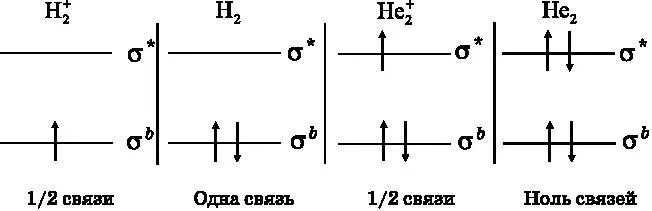
Рис. 12.9. Диаграмма энергетических уровней МО для четырёх молекул: молекулярного иона водорода H 2 + , молекулы водорода H 2 , молекулярного иона гелия He 2 + и молекулы He 2
Молекулярный ион He 2 +имеет три электрона. Первые два из них находятся на связывающей МО, но в силу принципа Паули третий электрон должен размещаться на разрыхляющей МО. Два электрона понижают энергию относительно раздельных атомов, но третий электрон повышает эту энергию. В целом имеет место уменьшение энергии. Молекулярный ион He 2 +существует в природе и имеет порядок связи, равный ½. Как уже говорилось, молекула He 2имеет два связывающих электрона и два разрыхляющих электрона. Связь не возникает, то есть порядок связи равен нулю. Молекулы He 2не существует.
В табл. 12.1 содержится количественная информация об этих четырёх молекулах. В ней приводятся число связывающих электронов, число разрыхляющих электронов и итоговый результат, равный разности числа связывающих электронов и числа разрыхляющих. В таблице также приводится порядок связи. Последние две колонки особенно интересны.
Таблица 12.1. Свойства молекулярного иона водорода H 2 + , молекулы водорода H 2 , молекулярного иона гелия He 2 + и молекулы He 2
Связ. электроны, Разр. электроны, Разность, Порядок связи, Длина связи, Энергия связи
H 2: 2; 0; 2; 1; 0,74Å; 7,2∙10 −19 Дж
H 2 +: 1; 0; 1; ½; 1,06Å; 4,2∙10 −19 Дж
He 2 +: 2; 1; 1; ½; 1,08Å; 5,4∙10 −19 Дж
He 2: 2; 2; 0; 0; Нет; Нет
Данные, приведённые в табл. 12.1, — это результаты экспериментальных измерений. Прежде всего, остановимся на длине химической связи. Она выражена в ангстремах (1 Å = 10 −10 м ). Молекулярный ион H 2 +имеет связь порядка ½ и длину химической связи 1,06 Å. Для сравнения отметим, что молекула H 2имеет полноценную связь порядка 1 и длину химической связи 0,74 Å. Дополнительный электрон на связывающей МО в молекуле H 2удерживает атомы крепче и потому теснее. Молекулярный ион He 2 +имеет связь порядка ½ и длину химической связи 1,08 Å, которая лишь незначительно больше, чем у молекулярного иона H 2 +. Конечно, He 2— это не молекула и поэтому не имеет химической связи. В последнем столбце приведена энергия связи в единицах 10 −19 Дж . Интересна относительная сила связи. Молекула H 2со связью порядка 1 имеет существенно бо́льшую энергию связи, чем два молекулярных иона, в которых порядок связи составляет ½. Так простые диаграммы МО позволяют узнать, будет ли существовать связь, и дают информацию о том, насколько сильной она окажется.
В этой главе мы воспользовались представлениями о молекулярных орбиталях для рассмотрения простейших молекул. Обсуждение касалось только атомов, содержащих 1 s -электроны. Все остальные атомы и молекулы содержат больше электронов и больше орбиталей. В следующей главе представленные здесь идеи будут использоваться для анализа двухатомных молекул, включающих более крупные атомы, такие как молекула кислорода O 2и молекула азота N 2. Эти две молекулы являются основными составляющими воздуха, которым мы дышим.
Читать дальшеИнтервал:
Закладка:










