Ричард Фейнман - 8. Квантовая механика I
- Название:8. Квантовая механика I
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ричард Фейнман - 8. Квантовая механика I краткое содержание
8. Квантовая механика I - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
что не должно меняться со временем. Если это обязано выполняться для любого начального условия j, то уравнение (6.40) тоже должно соблюдаться.
В качестве первого примера возьмем случай, когда физические условия не меняются со временем; мы имеем в виду внешние физические условия, так что Н не зависит от времени никаких магнитов никто не включает и не выключает. Выберем также систему, для описания которой хватает одного базисного состояния; такое приближение годится для покоящегося атома водорода и сходных систем. Уравнение (6.39) тогда утверждает, что

Только одно уравнение — и все! Если Н 11постоянно, это дифференциальное уравнение легко решается, давая
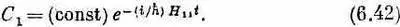
Так зависит от времени состояние с определенной энергией Е=Н 11 . Вы видите, почему Н ij следовало бы называть энергетической матрицей: она обобщает понятие энергии на более сложные случаи.
Вслед за этим, чтобы еще лучше разобраться в смысле уравнений, рассмотрим систему с двумя базисными состояниями.
Тогда (6.39) читается так:
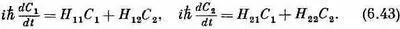
Если все Н опять не зависят от времени, то эти уравнения легко решить. Для интереса займитесь этим сами, а мы позже еще вернемся к ним. Вот вы уже и можете вести расчеты по квантовой механике, зная об Н только то, что оно не зависит от времени!
§ 6. Молекула аммиака
Теперь мы хотим продемонстрировать, как динамическое уравнение квантовой механики может быть использовано для описания какой-то физической обстановки. Мы выбрали интересный и простой пример, в котором, сделав некоторые разумные предположения о гамильтониане, сможем вывести кое-какие важные (и даже практически важные) результаты. Возьмем случай, когда достаточно двух состояний,— это молекула аммиака.
Молекулу аммиака образуют один атом азота и три атома водорода, плоскость которых проходит мимо атома азота, так что молекула имеет форму пирамидки (фиг. 6.1, а).
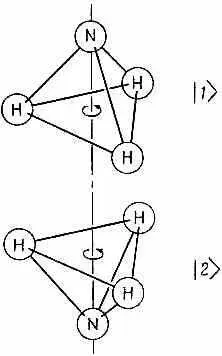
Фиг. 6.I. Два равноценных геометрических расположения молекулы аммиака.
Эта молекула, как и всякая другая, обладает бесконечным количеством состояний. Она может вращаться вокруг какой угодно оси; двигаться в любом направлении, вибрировать и т. д. и т. п. Значит, это вовсе не система с двумя состояниями. Но мы сделаем следующее приближение: предположим, что все прочие степени свободы закреплены и не связаны с теми, которые нас сейчас интересуют. Будем считать, что молекула может только вращаться вокруг оси симметрии (как показано на рисунке), что импульс ее переносного движения равен нулю и что ее колебания очень слабы. Это фиксирует все условия, кроме одного: для, атома азота все еще существуют два возможных положения — он может оказаться по одну сторону плоскости атомов водорода, а может оказаться и по другую (фиг. 6.1). Так что мы будем рассуждать о молекуле, как если бы она была системой с двумя состояниями. Под этим подразумевается, что существуют только два состояния, о которых реально следует заботиться, все же прочее предполагается зафиксированным. Как видите, если даже известно, что молекула вращается вокруг оси с определенным моментом количества движения и что она движется с определенным импульсом и колеблется определенным образом, то все равно еще остаются два Допустимых состояния. Будем говорить, что молекула находится в состоянии |1>, когда азот «вверху» (фиг. 6.1, а) и в состоянии |2>, когда азот «внизу» (фиг. 6.1, б). Состояния | 1 > и | 2 > в нашем анализе поведения молекулы аммиака можно принять за совокупность базисных состояний В каждый момент истинное состояние |y> молекулы может быть представлено заданием C 1=<1|y> — амплитуды пребывания в состоянии \1 и С 2=<2|y> — амплитуды пребывания в состоянии |2>. Тогда, используя (6.8), вектор состояния |y> можно записать так:
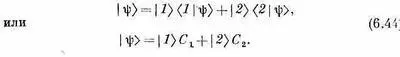
Но вот что интересно: если известно, что молекула в определенный момент была в определенном состоянии, то в следующий момент она может уже не быть в том же состоянии. Два С -коэффициента меняются со временем в соответствии с уравнениями (6.43), которые верны для любой системы с двумя состояниями. Предположим, к примеру, что вы сделали какое-то наблюдение (или как-то отобрали молекулы), так что знаете, что первоначально молекула находилась в состоянии |1>. Чуть позже уже появляются некоторые шансы засечь ее в состоянии |2>. Чтобы узнать, сколь велики эти шансы, нужно решить дифференциальное уравнение, которое говорит, как амплитуды меняются со временем.
Единственная трудность в том, что мы не знаем, что ставить вместо коэффициентов Н ij в (6.43). Но кое-что мы все же можем сказать. Предположим, что, если уж молекула оказалась в состоянии \1 >, тогда у нее не будет никакого шанса когда-либо попасть в состояние |2>, И наоборот. Тогда H 12и H 21будут оба равны нулю, и (6.43) примет вид
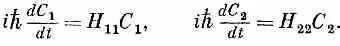
Эти уравнения легко решить; получается
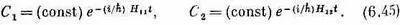
Это просто амплитуды стационарных состояний с энергиями E 1 =H 11и E 2= H 22. Еще мы знаем, что у молекулы аммиака состояния | 1>и | 2>обладают определенной симметрией. Если природа ведет себя более или менее разумно, то матричные элементы Н 11и H 22должны равняться друг другу. Мы обозначим их через Е 0 , потому что они соответствуют энергии, которой обладали бы состояния, будь H 12и H 21равны нулю.
Но (6.45) не отражает того, что на самом деле бывает с аммиаком. Оказывается, что аммиак имеет возможность протолкнуть свой азот мимо трех водородов и перебросить его по ту сторону. Это очень трудно: чтобы азоту пройти полпути, нужна немалая энергия. Как же он может пройти на другую сторону, если он не располагает достаточной энергией? Просто имеется некоторая амплитуда того, что он проникнет сквозь энергетический барьер. В квантовой механике разрешается быстро проскакивать через энергетически нелегальную область. Стало быть, существует небольшая амплитуда того, что молекула, начав с состояния |1>, перейдет в состояние |2>. Коэффициенты Н 12и Н 21на самом деле не равны нулю. И опять из симметрии ясно, что они должны быть одинаковы, по крайней мере по величине. И действительно, мы уже знаем, что вообще Н ij равняется комплексно сопряженной величине Н ji , т. е, они могут отличаться только фазой. Оказывается, как вы потом увидите, что без потери общности можно положить эти коэффициенты равными друг другу. Позднее нам будет удобнее считать их равными отрицательному числу; мы примем поэтому H 12= H 21=- А. Тогда получится следующая пара уравнений:
Читать дальшеИнтервал:
Закладка:






