Никита Кривушкин - Пособие по изучению иммунного ответа. Патофизиология TLR и её влияние на механизмы развития патогенеза заболеваний иммунной системы
- Название:Пособие по изучению иммунного ответа. Патофизиология TLR и её влияние на механизмы развития патогенеза заболеваний иммунной системы
- Автор:
- Жанр:
- Издательство:Литагент Ридеро
- Год:неизвестен
- ISBN:9785448560217
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Никита Кривушкин - Пособие по изучению иммунного ответа. Патофизиология TLR и её влияние на механизмы развития патогенеза заболеваний иммунной системы краткое содержание
Пособие по изучению иммунного ответа. Патофизиология TLR и её влияние на механизмы развития патогенеза заболеваний иммунной системы - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Генетический вариант в TLR1 может способствовать низкое тяжелой малярии коэффициент летальности в этой области, за счет снижения провоспалительного клеточного фенотипа.
Данное исследование проводилось с целью определения влияния TLR-1 на патогенез механизмов аллергии.
TLR-1/2 в периферической крови мононуклеарных клеток и моноцит-производных дендритных клеток разных генотипов были измерены с помощью твердофазного иммуноферментного анализа (ИФА). 93 тайваньских пациента, страдающих аллергией (бронхиальная астма, аллергический ринит или атопический дерматит) были привлечены для генотипирования. Сыворотка иммуноглобулина Е (IgE) уровень были оценены для 60 пациентов, страдающих аллергией.
TLR1 несущей аллель возросло Pam3CSK4-индуцированного фактора некроза опухоли-α и интерлейкина-12 ответов в периферической крови мононуклеарных клеток и моноцит-производных дендритных клеток, соответственно. Кроме того, хотя Генотип С/С не был связан с восприимчивостью к атопическим заболеваниям, это сопровождается снижением уровня общего IgE в сыворотках крови пациентов, страдающих аллергией.
Наши данные свидетельствуют о том, что TLR1 полиморфизм может играть роль в формировании th1/Тһ2-дифференцировки, и определение сывороточного уровня IgE. Однако, взаимодействия с другими генетическими и экологическими факторами может потребоваться внести вклад в риск возникновения аллергических заболеваний у населения.
Можно обнаружить в зараженных перипротезных тканях TLR и оценить полезность этих биомаркеров в качестве тестов для выявления перипротезной инфекции.
Пятьдесят девять пациентов, перенесших пересмотра эндопротезировании (двадцать семь бедра и тридцать два колена) были перспективно оценены по перипротезной инфекции в соответствии с рекомендуемыми в настоящее время диагностическими критериями. Девять пациентов были исключены из-за нехватки работы, оставив пятьдесят доступны для изучения.. Перипротезные ткани были собраны интраоперационно, и тотальную РНК выделяли по стандартным методикам. Экспрессию ТЛР-мессенджер РНК оценивали по первой нити комплементарной синтез ДНК 1 мкг тотальной РНК с последующим ПЦР в реальном времени (полимеразная цепная реакция).
TLR1 экспрессия мРНК была значительно выше в инфицированных по сравнению с незараженных образцов (0.600 по сравнению с 0,005, р = 0.0003); то же самое касается TLR6 (0.208 по сравнению с 0.0165, р = 0.0059), но не TLR10 (0.00019 по сравнению с 0.00014, р = 0.6238). Аук был 0.995 для TLR1, TLR6 для 0.883, и 0.546 для TLR10. Оптимальный порог для диагностики перипротезной инфекции 0.0924 для TLR1 (чувствительность = 95.2%, специфичность = 100%, ОП+ = 13.80, ЛР- = 0.91) и 0.0215 для TLR6 (чувствительность = 85.7%, специфичность = 82.8%, ОП+ = 4.98, ЛР- = 0.83).
В нашем экспериментальном исследовании, TLR1 выраженны в перипротезные ткани и наиболее точно предсказывали перипротезные инфекции. Эта мера реакции хозяина могут быть особенно полезны в обнаружении культура-отрицательных инфекций.
Инфекции нижних дыхательных путей, вызванных бактериями являются основной причиной смерти людей независимо от пола, расы, или географии. Действительно, накопленные данные свидетельствуют о более высокой смертности и заболеваемости из-за этих инфекций, чем от рака, малярии или ВИЧ-инфекции. Успешное признание, за которым последует соответствующий ответ, бактериальных патогенов в легких имеет решающее значение для эффективного легочного узла обороны. Хотя активация нейтрофилов в легких является ключевым фактором в ответе от вторжения микробов-возбудителей, альвеолярные макрофаги, эпителиальные клетки, дендритные клетки и CD4 (+) Т-клеток, также способствует ликвидации бактериальной нагрузки. Распознавания образов рецепторы, такие как toll-подобные рецепторы (tlrs) и нуклеотид-связывающий домен олигомеризации-подобных рецепторов, имеют важное значение для признания и учета микроорганизмов в легочной инфекции. Однако, бактериальные патогены приобрели хитрую уклончивую стратегию, чтобы обойти распознавание отклика рецептора и таким образом создать инфекции. Углубление понимания функции системы tlrs и уклончиво механизмов, используемых микроорганизмами в легочной инфекцией позволит углубить наши знания об иммунопатогенезе и имеет решающее значение для разработки эффективных терапевтических и/или профилактических мер. В настоящем обзоре обобщены современные знания несколько ролей системы tlrs в бактериальные инфекции легких и основные механизмы, используемые патогенными для модуляции или мешать ТЛР сигнализации в легких.
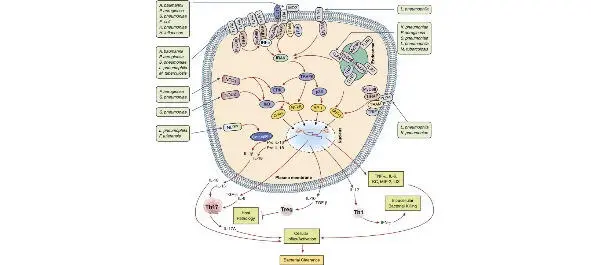
Сигнальный каскад при активации распознавания рецепторов легочных патогенов.Плазматическая мембрана-граница Толл-подобных рецепторов (tlrs) (TLR1, 2, 4, 5) и мембраносвязанных температуры окружающей среды системы tlrs (TLR9) распознает бактерии в легких. После этого происходит активация фактора транскрипции ядерного фактора-кв (NF-кВ) и митоген-активируемых протеинкиназ (MAPKs). АП-1 активацию Map-киназного каскада, в свою очередь, приводит к индукции транскрипционных факторов и C-ФОС. Кроме того, при стимуляции лигандами, в NOD-подобного рецептора белка (NLRP) индуцируют активацию эффекторной каспазы-1. В свою очередь, ведет к активации цитокинов в дифференцировке Т-клеток на th1 -, th17-лимфоцитов, или регуляторные Т-клетки (Tregs), что приводит к формированию легочного узла обороны.
А. baumannii = инфекциями, вызванными acinetobacter baumannii; е. coli = кишечная палочка; Ф. название рода = мелкая грамотрицательная палочка; культура H. influenzae = Гемофильная инфекция; К. рпеимопіае = Клебсиелла пневмонии; л. pneumophila = Легионеллы pneumophila; микобактерии туберкулеза = микобактерий туберкулеза; клеток P. aeruginosa = Синегнойная палочка; С. рпеимопіае = пневмококк.
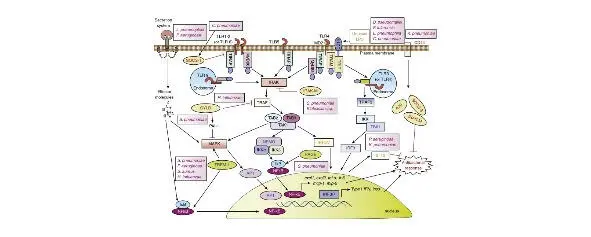
Сигнализация при бактериальных инфекциях легких
Негативные регуляторы системы tlrs (показано красным цветом бледно-зеленые эллипсы), ил-1 рецептор-ассоциированной киназы-М (Ирак-М), супрессоры цитокиновых сигналов 1 (МНК-1), предназначенные для разных молекул внутри ТЛР сигнального пути для подавления их экспрессии или активации.
Положительные регуляторы (показаны синим цветом на темно-зеленых эллипсах), срабатывающие на миелоидные клетки 1 (ТРЭМ-1), рецептор для конечных продуктов гликирования, секреторные молекулы бактериальной системы секреции, усиливают ТЛР срабатывания сигнализации путем активации ядерного фактора (НФ) -KB и/или митоген-активируемых протеинкиназ (MAPKs).
Б. псевдоволосы = отличает псевдоволосы; С. рпеимопіае = хламидии пневмонии; Ф. название рода = мелкая грамотрицательная палочка; культура H. influenzae = Гемофильная инфекция; К. рпеимопіае = Клебсиелла пневмонии; л. pneumophila = Легионеллы pneumophila; П. аегидіпоѕа = Синегнойная палочка; золотистый стафилококк = стафилококк; С. рпеимопіае = пневмококк.
Читать дальшеИнтервал:
Закладка:










