Александр Артеменко - Удивительный мир органической химии
- Название:Удивительный мир органической химии
- Автор:
- Жанр:
- Издательство:Дрофа
- Год:2005
- Город:Москва
- ISBN:5-7107-9540-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Александр Артеменко - Удивительный мир органической химии краткое содержание
Книга адресована старшеклассникам, учителям, а также тем, кто интересуется органической химией.
Удивительный мир органической химии - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Хорошо известно, что в симметрично построенных молекулах (метан СН 4, четыреххлористый углерод СCl 4и др.) четыре связи углерода практически одинаковы. Это происходит потому, что для атома крайне невыгодно, если его связи образованы электронами с различной энергией. Не только математический подход, но даже здравый смысл говорит о том, что в молекуле, например, метана электроны находятся не на «чистых» 2 s- и 2 p -орбиталях, а на смешанных — гибридных. Такие орбитали симметрично расположены в пространстве и имеют одинаковую энергию. Процесс образования гибридных орбиталей химики назвали гибридизацией.
Для атома углерода возможны три типа гибридизации. Рассмотрим их подробнее.
Первый тип гибридизации — sp 3- гибридизация. Она происходит при «смешении» (комбинации) одной 2 s -орбитали и трех 2 p -орбиталей. В результате образуются четыре одинаковые sp 3 -гибридные орбитали, каждая из которых имеет грушевидную форму (одна часть «гантели» стала вытянутой в одну сторону от ядра) (рис. 8).
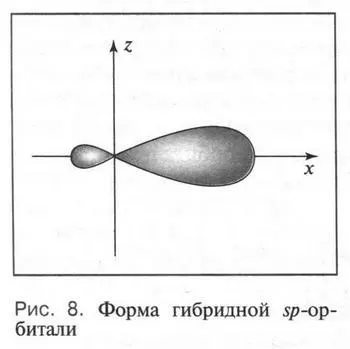
Такая форма очень выгодна. При образовании химических связей она способствует более полному перекрыванию с орбиталями других атомов. А чем полнее такое перекрывание, тем прочнее химическая связь. В пространстве четыре sp 3-гибридные орбитали строго ориентированы друг относительно друга и образуют своими утолщенными областями геометрическую фигуру — тетраэдр. Поэтому углы между осями гибридных орбиталей составляют 109°28' (рис. 9). Углеродный атом с sp 3-гибридными орбиталями участвует в образовании соединений с простой связью: метана, этана, пропана и подобных им углеводородов — алканов.
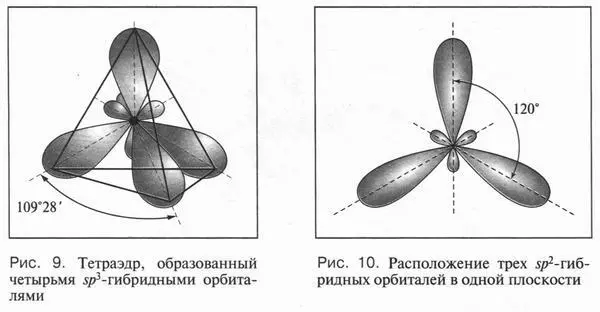
Второй тип гибридизации — sp 2 -гибридизация. При «смешении» одной 2 s- и двух 2 p -орбиталей образуются три одинаковые sp 2-гибридные орбитали. Они располагаются в одной плоскости под утлом 120° друг к другу (рис. 10). Третья 2 p -орбиталь не вступает в гибридизацию и сохраняет свою обычную форму. Эта орбиталь располагается в плоскости, которая перпендикулярна плоскости трех гибридных орбиталей (рис. 11). Этот тип гибридизации характерен для углерода, который входит в состав соединений с двойной связью — алкенов (например, этилена, пропилена и др.).
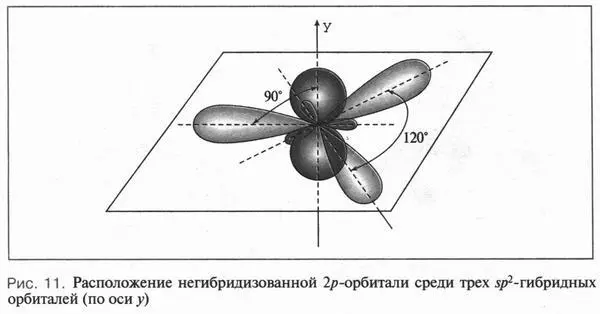
И наконец, sp-гибридизация. Она происходит при «смешении» одной 2 s- и одной 2 p -орбитали. В результате образуются две одинаковые sp- гибридные орбитали. Они расположены на одной линии под утлом 180° друг к другу (рис. 12). Две другие 2 p -орбитали остаются негибридизованными и располагаются во взаимно перпендикулярных плоскостях (рис. 13). Такая гибридизация характерна для углеводородов с тройной связью — алкинов (например, ацетилена).
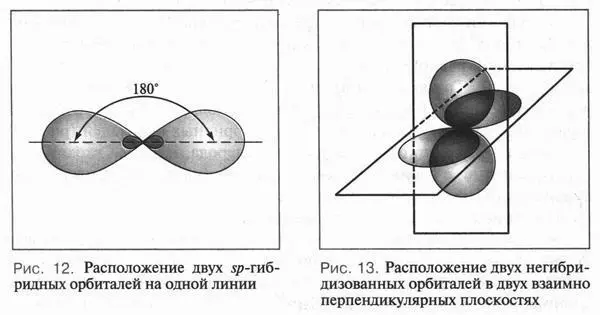
Происходит ли процесс гибридизации в действительности? Нет. Это лишь математический прием, гипотеза химиков-теоретиков, не подтвержденная экспериментально. Но теория гибридизации оказала большую услугу химикам. Она позволяет объяснить характер образующихся связей, их особенности, но главное — показать пространственное строение многих органических молекул.
Глава 3
Молекулы из двух элементов

3.1. Тетраэдр — «подарок» природы
Вот мы и узнали, как устроен атом углерода — главный элемент органического мира. Теперь перейдем к знакомству с наиболее простыми органическими веществами. Самым известным органическим соединением является метан. Вот формула его молекулы:
Метан — не только земное, но и космическое вещество: он содержится в атмосфере Сатурна и Юпитера, а в твердом состоянии его обнаружили на Уране и Нептуне. Метан по праву можно назвать «Адамом органического мира». Заменив в его молекуле один или несколько водородных атомов на другие атомы или группы атомов, можно получить многие органические соединения.
Метан — главная составная часть природного (до 98%) газа, а также попутных газов, которые выделяются при добыче нефти. В значительных количествах он присутствует в газах нефтепереработки. Обнаружить метан можно даже в любом болоте или пруду. Если палочкой пошевелить ил, то на поверхность воды поднимутся пузырьки болотного газа, который в основном состоит из метана. Он образовался из погибших растений и других веществ под воздействием особых бактерий без доступа воздуха.
Мы ежедневно встречаемся с метаном. Его используют в качестве дешевого топлива в быту и в промышленности. Метан — газ без цвета и запаха. Поэтому, пользуясь метаном, необходимо быть очень осторожным. Он образует с воздухом взрывоопасную смесь. Обычно для обнаружения утечки метана в газопроводах к нему добавляют небольшое количество сильно пахнущего вещества. Обычно с этой целью применяют газообразные тиоспирты (меркаптаны). Особенно опасен метан в шахтах («рудничный газ»). Взрывы метана в шахтах стоили жизни многим тысячам шахтеров.
Какое строение имеет молекула метана? Ответить на этот вопрос нам поможет теория гибридизации.
Как вы помните, в молекуле метана атом углерода находится в состоянии sp 3-гибридизации. Это означает, что атом имеет четыре одинаковые sp 3-гибридные орбитали, направленные в пространстве под углом 109°28' друг к другу (рис. 14). Если представить атом углерода центром молекулы, то эти орбитали будут направлены к вершинам правильного тетраэдра. Перекрываясь с четырьмя орбиталями атомов водорода (в атоме водорода единственный электрон занимает шаровую 1 s -орбиталь), углеродные орбитали образуют четыре одинаковые связи С—Н. Следует отметить, что перекрывание орбиталей при этом происходит по линии, соединяющей ядра атомов углерода и водорода. Такие химические связи принято называть σ(сигма)-связями, а электроны, образующие их, — σ-электронами.
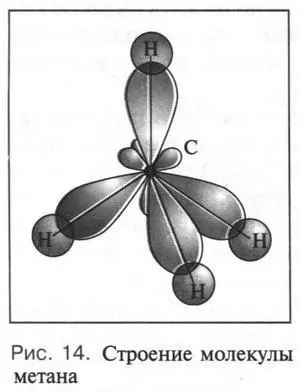
Разве не удивительно, что одна из тайн природы состоит в том, что в качестве основного геометрического элемента для органической химии она избрала тетраэдр!
Читать дальшеИнтервал:
Закладка:









