Александр Артеменко - Удивительный мир органической химии
- Название:Удивительный мир органической химии
- Автор:
- Жанр:
- Издательство:Дрофа
- Год:2005
- Город:Москва
- ISBN:5-7107-9540-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Александр Артеменко - Удивительный мир органической химии краткое содержание
Книга адресована старшеклассникам, учителям, а также тем, кто интересуется органической химией.
Удивительный мир органической химии - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Мы уже говорили, что химики с успехом используют теорию гибридизации для предсказания пространственной формы многих органических молекул. Например, эта теория довольно точно предсказала величины углов между связями в молекуле метана, а также расположение этих связей в молекуле.
Метан — самое распространенное и доступное химикам вещество. В промышленности его получают из природного газа или нефти. Можно получить метан и в лаборатории, например взаимодействием карбида алюминия с водой:

Можно получать метан и при нагревании оксида углерода (II) с водородом в присутствии катализатора:

Однако синтетическим путем метан обычно не получают. В этом нет необходимости, поскольку природный газ состоит практически из метана.
Метан служит прекрасным сырьем для получения многих органических соединений. Мы узн а ем об этом, если познакомимся с химическими свойствами этого простого, но удивительного вещества.
Метан относится к органическим соединениям, которые проявляют очень низкую химическую активность. Эти соединения в свое время получили название парафины (от лат. parum affinis — малоактивный). В настоящее время их называют алканами. Метан — самый первый и самый важный представитель класса этих веществ, которые образуют особый ряд, названный гомологическим (от греч. homós — равный, одинаковый). Вещества, составляющие этот ряд, являются гомологами. Первым в этом ряду стоит метан. За метаном следует этан, потом — пропан, бутан, пентан и т. д. Все эти вещества подчиняются общей формуле С nН 2n+2. Это очень удобная формула. Зная количество атомов углерода в алкане, можно сразу же сказать, сколько в молекуле будет атомов водорода.
Метан и его гомологи (т. е. этан, пропан, бутан, пентан и др.) не взаимодействуют при обычных условиях с кислотами, щелочами, окислителями. Недаром же когда-то эти вещества назвали «химическими мертвецами». И все же химики «приручили» эти соединения. Они заставили их вступать в некоторые реакции. В основном это реакции замещения , при которых происходит замена атомов водорода на другие атомы. Сразу же скажем, что в реакции присоединения (когда к одному веществу присоединяется другое) алканы вступать не могут. И дело тут не в том, что они «капризны». Их углеродные атомы полностью насыщены, т. е. у них нет возможностей присоединять. Действительно, если атом углерода может образовать только четыре связи с другими атомами, то образовать пятую связь он не в состоянии.
Какие же реакции замещения характерны для алканов?
Известно, что при освещении или нагревании метан очень бурно реагирует с хлором. Ученые изучили эту реакцию и выяснили, что она начинается с распада молекулы хлора на два атома хлора. Эти атомы на внешней электронной оболочке имеют один неспаренный электрон. Атомы или группы атомов с таким «лишним» электроном называются свободными радикалами. Распад молекулы хлора при соответствующих условиях на два свободных радикала (два атома хлора) можно изобразить так:

В молекуле хлора точками обозначены электронные пары, а в атоме хлора (справа) показан неспаренный электрон. Такой атом (радикал) обладает высокой энергией. Атакуя молекулу метана, он отрывает от нее водородный атом.
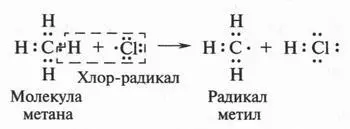
В результате такого отрыва образуется новая активная частица — радикал метил (•СН 3). Этот радикал очень быстро (он существует в свободном состоянии тысячные доли секунды) взаимодействует с молекулой хлора, расщепляя ее на две части. В результате образуются молекула хлорметана и снова хлор-радикал:
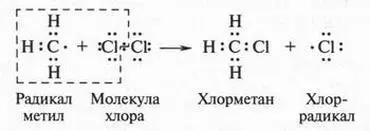
И все повторяется снова: хлор-радикал атакует новые молекулы метана с образованием метильных радикалов, а те, в свою очередь, «набрасываются» на молекулы хлора. Поскольку в результате таких последовательных реакций образуются свободные радикалы, то весь процесс называется свободнорадикальным. Такие реакции называют также цепными, так как одна стадия реакций связана с другой как звенья одной цепи.
Открытие таких реакций было одним из выдающихся событий в химии. За огромный вклад в изучение цепных реакций и создание их теории академик Николай Николаевич Семенов (1896-1986)  и английский химик Сирил Норман Хиншелвуд (1897-1967) были удостоены в 1956 г. высшей научной награды — Нобелевской премии.
и английский химик Сирил Норман Хиншелвуд (1897-1967) были удостоены в 1956 г. высшей научной награды — Нобелевской премии.
Итак, в результате замещения атома водорода на атом хлора образуется хлорпроизводное метана — хлорметан (или иначе — хлористый метил, газообразное вещество, которое можно применять в холодильных установках в качестве хладагента).
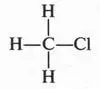
Однако реакция метана с хлором может идти и дальше. Все водородные атомы в молекуле метана можно заместить на атомы хлора. Вот как это выглядит:
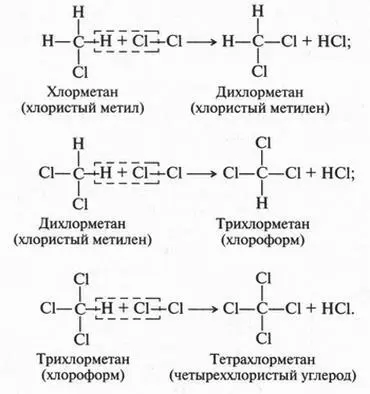
Точно так же с метаном реагирует и бром. Что же касается иода, то при непосредственном взаимодействии его с метаном иодпроизводные получить не удается. А вот фтор с метаном и подобными ему соединениями (алканами) реагирует настолько активно, что эту реакцию можно назвать взрывом. Это происходит потому, что фтор даже при нормальной температуре легко распадается на свободные фтор-радикалы.
Все эти реакции называются реакциями галогенирования, а продукты, получаемые при этих реакциях, носят название галогенопроизводных.
Галогенопроизводные метана (и его гомологов) — химически активные вещества. Из них получают многие органические соединения. Например, если на йодистый метил (иодметан) подействовать металлическим натрием, то получим этан:
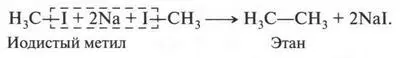
Эту реакцию открыл в 1855 г. французский химик Шарль Адольф Вюрц (1817-1884). С помощью этой реакции можно получать различные предельные углеводороды (алканы).
Читать дальшеИнтервал:
Закладка:









