БСЭ БСЭ - Большая Советская Энциклопедия (МА)
- Название:Большая Советская Энциклопедия (МА)
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
БСЭ БСЭ - Большая Советская Энциклопедия (МА) краткое содержание
Большая Советская Энциклопедия (МА) - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Магний
Ма'гний(лат. Magnesium), Mg, химический элемент II группы периодической системы Менделеева, атомный номер 12, атомная масса 24,305. Природный М. состоит из трёх стабильных изотопов: 24Mg (78,60% ), 25Mg (10,11%) и 26Mg (11,29%). М. открыт в 1808 Г. Дэви, который подверг электролизу с ртутным катодом увлажнённую магнезию (давно известное вещество); Дэви получил амальгаму, а из неё после отгонки ртути — новый порошкообразный металл, названный магнием. В 1828 французский химик А. Бюсси восстановлением расплавленного хлорида М. парами калия получил М. в виде небольших шариков с металлическим блеском.
Распространение в природе. М. — характерный элемент мантии Земли, в ультраосновных породах его содержится 25,9% по массе. В земной коре М. меньше, средний кларк его 1,87%; преобладает М. в основных породах (4,5%), в гранитах и других кислых породах его меньше (0,56%). В магматических процессах Mg 2+— аналог Fe 2+, что объясняется близостью их ионных радиусов (соответственно 0,74 и 0,80 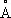 ). Mg 2+вместе с Fe 2+входит в состав оливина, пироксенов и других магматических минералов.
). Mg 2+вместе с Fe 2+входит в состав оливина, пироксенов и других магматических минералов.
Минералы М. многочисленны — силикаты, карбонаты, сульфаты, хлориды и другие (см. Магниевые руды ) . Более половины из них образовались в биосфере — на дне морей, озёр, в почвах и т. д.; остальные связаны с высокотемпературными процессами.
В биосфере наблюдается энергичная миграция и дифференциация М.; здесь главная роль принадлежит физико-химическим процессам — растворению, осаждению солей, сорбции М. глинами. М. слабо задерживается в биологическом круговороте на континентах и с речным стоком поступает в океан. В морской воде в среднем 0,13% М. — меньше, чем натрия, но больше всех других металлов. Морская вода не насыщена М. и осаждения его солей не происходит. При испарении воды в морских лагунах в осадках вместе с солями калия накапливаются сульфаты и хлориды М. В илах некоторых озёр накапливается доломит (например, в озере Балхаш). В промышленности М. получают в основном из доломитов, а также из морской воды.
Физические и химические свойства. Компактный М. — блестящий серебристо-белый металл, тускнеющий на воздухе вследствие образования на поверхности окисной плёнки. М. кристаллизуется в гексагональной решётке, а = 3,2028 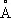 , с = 5,1998
, с = 5,1998 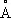 . Атомный радиус 1,60
. Атомный радиус 1,60 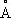 , ионный радиус Mg 2+0,74
, ионный радиус Mg 2+0,74 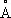 . Плотность М. 1,739 г/см 3 (20 °С); t пл 651 °С; t kип 1107 °С. Удельная теплоёмкость (при 20 °С) 1,04×10 3 дж/(кг·К) , то есть 0,248 кал/(г·°С) ; теплопроводность (20 °С) 1,55×10 2 вт/(м·К) , то есть 0,37 кал/(см·сек·°С) ; термический коэффициент линейного расширения в интервале 0—550 °С определяется из уравнения 25,0×10 -6+ 0,0188 t . Удельное электрическое сопротивление (20 °С) 4,5×10 -8 ом·м (4,5 мком·см ) . М. парамагнитен, удельная магнитная восприимчивость + 0,5×10 -6, М. — относительно мягкий и пластичный металл; его механические свойства сильно зависят от способа обработки. Например, при 20 °С свойства соответственно литого и деформированного М. характеризуются следующими величинами: твёрдость по Бринеллю 29,43×10 7и 35,32× 10 7 н/м 2 (30 и 36 кгс/мм 2 ) , предел текучести 2,45×10 7и 8,83×10 7 н/м 7 (2,5 и 9,0 кгс/мм 2 ) , предел прочности 11,28×10 7и 19,62×10 7 н/м 2 (11,5 и 20,0 кгс/мм 2 ) , относительное удлинение 8,0 и 11,5%.
. Плотность М. 1,739 г/см 3 (20 °С); t пл 651 °С; t kип 1107 °С. Удельная теплоёмкость (при 20 °С) 1,04×10 3 дж/(кг·К) , то есть 0,248 кал/(г·°С) ; теплопроводность (20 °С) 1,55×10 2 вт/(м·К) , то есть 0,37 кал/(см·сек·°С) ; термический коэффициент линейного расширения в интервале 0—550 °С определяется из уравнения 25,0×10 -6+ 0,0188 t . Удельное электрическое сопротивление (20 °С) 4,5×10 -8 ом·м (4,5 мком·см ) . М. парамагнитен, удельная магнитная восприимчивость + 0,5×10 -6, М. — относительно мягкий и пластичный металл; его механические свойства сильно зависят от способа обработки. Например, при 20 °С свойства соответственно литого и деформированного М. характеризуются следующими величинами: твёрдость по Бринеллю 29,43×10 7и 35,32× 10 7 н/м 2 (30 и 36 кгс/мм 2 ) , предел текучести 2,45×10 7и 8,83×10 7 н/м 7 (2,5 и 9,0 кгс/мм 2 ) , предел прочности 11,28×10 7и 19,62×10 7 н/м 2 (11,5 и 20,0 кгс/мм 2 ) , относительное удлинение 8,0 и 11,5%.
Конфигурация внешних электронов атома М. 3s 2. Во всех стабильных соединениях М. двухвалентен. В химияеском отношении М. — весьма активный металл. Нагревание до 300—350 °C не приводит к значительному окислению компактного М., так как поверхность его защищена окисной плёнкой, но при 600—650 °C М. воспламеняется и ярко горит, давая магния окись и отчасти нитрид Mg 3N 2. Последний получается и при нагревании М. около 500 °С в атмосфере азота. С холодной водой, не насыщенной воздухом, М. почти не реагирует, из кипящей медленно вытесняет водород; реакция с водяным паром начинается при 400 °C. Расплавленный М. во влажной атмосфере, выделяя из H 2O водород, поглощает его; при застывании металла водород почти полностью удаляется. В атмосфере водорода М. при 400—500 °C образует MgH 3.
М. вытесняет большинство металлов из водных растворов их солей; стандартный электродный потенциал Mg при 25 °С — 2,38 в. С разбавленными минеральными кислотами М. взаимодействует на холоду, но в плавиковой кислоте не растворяется вследствие образования защитной плёнки из нерастворимого фторида MgF 2. В концентрированной H 2SO 4и смеси её с HNO 3М. практически нерастворим. С водными растворами щелочей на холоду М. не взаимодействует, но растворяется в растворах гидрокарбонатов щелочных металлов и солей аммония. Едкие щёлочи осаждают из растворов солей М. гидроокись Mg(OH) 2, растворимость которой в воде ничтожна. Большинство солей М. хорошо растворимо в воде, например магния сульфат; мало растворимы MgF 2, MgCO 3(см. Магния карбонат ) , Mg 3(PO 4) 2и некоторые двойные соли.
При нагревании М. реагирует с галогенами, давая галогениды; с влажным хлором уже на холоду образуется MgCl 2. При нагревании М. до 500—600 °С с серой или с SO 2и H 2S может быть получен сульфид MgS, с углеводородами — карбиды MgC 2и Mg 2C 3. Известны также силициды Mg 2Si, Mg 3Si 2, фосфид Mg3P 2и другие бинарные соединения. М. — сильный восстановитель; при нагревании вытесняет другие металлы (Be, Al, щелочные) и неметаллы (В, Si, С) из их окислов и галогенидов. М. образует многочисленные металлоорганические соединения, определяющие его большую роль в органическом синтезе (см. Магнийорганические соединения ) . М. сплавляется с большинством металлов и является основой многих технически важных лёгких сплавов.
Получение и применение. В промышленности наибольшее количество М. получают электролизом безводного хлорида MgCl 2или обезвоженного карналлита KCl×MgCl 2×6H 2O (см. Магния хлорид ) . В состав электролита входят также хлориды Na, К, Са и небольшое количество NaF или CaF 2. Содержание MgCl 2в расплаве — не менее 5—7%; по мере хода электролиза, протекающего при 720—750 °С, проводят корректировку состава ванны, удаляя часть электролита и добавляя MgCl 2или карналлит. Катоды изготовляют из стали, аноды — из графита. Расплавленный М., всплывающий на поверхность электролита, периодически извлекается из катодного пространства, отделённого от анодного перегородкой, не доходящей до дна ванны. В состав чернового М. входят до 2% примесей; его рафинируют в тигельных электрических печах под слоем флюсов и разливают в изложницы. Лучшие сорта первичного М. содержат 99,8% Mg. Последующая очистка М. проводится сублимацией в вакууме: 2—3 сублимации повышают чистоту М. до 99,999%. Анодный хлор после очистки используется для получения безводного MgCl 2из магнезита, тетрахлорида титана TiCl 4из двухокиси TiO 2и других соединений.
Читать дальшеИнтервал:
Закладка:
