Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться
- Название:Против часовой стрелки. Что такое старение и как с ним бороться
- Автор:
- Жанр:
- Издательство:Альпина нон-фикшн
- Год:2020
- Город:Москва
- ISBN:978-5-0013-9314-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться краткое содержание
В своей книге биолог и научный журналист Полина Лосева выступает в роли адвоката современной науки о старении и рассказывает о том, чем сегодня занимаются геронтологи и как правильно интерпретировать полученные ими результаты. Кто виноват в том, что мы стареем? Что может стать нашей защитой от старости: теломераза или антиоксиданты, гормоны или диеты? Биологи пока не пришли к единому ответу на эти вопросы, и читателю, если он решится перейти от размышлений к действиям, предстоит сделать собственный выбор.
Эта книга станет путеводителем по современным теориям старения не только для биологов, но и для всех, кому интересно, как помочь своему телу вести неравную борьбу со временем.
Против часовой стрелки. Что такое старение и как с ним бороться - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Если внимательно посмотреть на список генов, которые позволяют объяснить разброс в продолжительности жизни у людей, то можно заметить, что большинство из них так или иначе связаны [604] Trimmers P. R. H. J. et al. Genomics of 1 million parent lifespans implicates novel pathways and common diseases and distinguishes survival chances // eLife. 2019; 8: e39856.
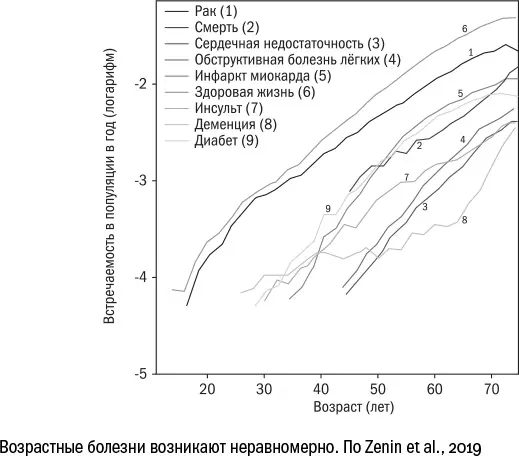
с основными рисками смерти в пожилом возрасте: деменцией, сердечно-сосудистыми болезнями и раком легких. Да и сами кривые смертности от возрастных болезней подозрительно напоминают [605] Zenin A. et al. Identification of 12 genetic loci associated with human healthspan // Communications Biology. 2019 Jan; 2: 41.
кривую Гомперца. Это позволяет предположить, что самая выигрышная стратегия для долгой жизни – избежать наиболее распространенных болезней. Но если это так, то набор генов, связанных с долголетием, будет меняться по мере развития медицины. В XIX веке люди чаще умирали от инфекций, чем сейчас, в XX веке на смену инфекциям пришли деменция и рак. Кто знает, когда мы научимся бороться и с ними, какая болезнь следующей выйдет на первый план? И тогда через сотню лет в статьях, посвященных долгожительству, будут значиться совсем другие гены.
Против логики
Долгие и безрезультатные поиски генов, которые отвечали бы за изнашивание организма, сильно подрывают позиции теории запрограммированного старения. Но это не единственный аргумент, который есть у противников этой теории [606] Kowald A. & Kirkwood T. B. L. Can aging be programmed? A critical literature review // Aging Cell. 2016 Aug; 15 (6): 986–998.
.
Еще, например, они требуют объяснить, как такая программа могла бы появиться [607] Gladyshev V. N. Aging: progressive decline in fitness due to the rising deleteriome adjusted by genetic, environmental, and stochastic processes // Aging Cell. 2016 Apr; 15 (4): 594–602.
. Владимир Скулачев, например, утверждает, что выбывание старых организмов из популяции ускоряет смену поколений и, следовательно, эволюцию вида. Но, если особь дожила до пожилого возраста, это значит, что она достаточно хорошо приспособлена к условиям, в которых существует. Имеет ли смысл убивать ее в надежде, что молодое поколение случайно окажется носителем еще более "удачных" для данных условий мутаций? Учитывая, что "удачные" мутации возникают нечасто, такая стратегия может не принести непосредственной выгоды для популяции – а значит, не будет поддержана отбором.
Другое соображение сторонников программируемого старения состоит в том, что чем короче поколение, тем больше генетических вариантов "проверяется" природой одновременно, то есть выше разнообразие и выше шанс "угадать" и получить подходящий генотип. Но если условия внешней среды не изменяются постоянно, то такая спешка не приносит непосредственной выгоды – предыдущее поколение может оказаться достаточно приспособленным. А если условия внешней среды изменяются все время, то пожилые особи, с которыми должна бы бороться программа, не успевают заполнить собой всю нишу и вытеснить оттуда молодое поколение.
Наконец, идея о том, что старшее поколение "объедает" младшее и забирает себе все ресурсы, тоже не выдерживает критики: она работает только в том случае, когда каждая особь слабо подвижна и спаривается только с близко расположенными партнерами. Тогда действительно оказывается важным освобождать место за счет гибели старых особей. Но если организмы достаточно крепки, чтобы перемещаться по своей территории, то этот аргумент теряет силу.
Впрочем, самым сильным все равно остается генетический довод: как бы ожесточенно сторонники программируемого старения ни искали кнопку "пуск", до сих пор пока ничего не нашли. Ни у человека, ни у мышей, ни у беспозвоночных нет такого гена, который позволил бы отменить старение. И даже животное, которое стало эмблемой теории программируемого старения – голый землекоп – не живет вечно и страдает [608] Delaney M. A., Kinsel M. J., Treuting P. M. Renal pathology in a nontraditional aging model: the naked mole-rat (Heterocephalus glaber) // Veterinary Pathology. 2016 Mar; 53 (2): 493–503.
возрастными болезнями [609] Edrey Y. H., Hanes M., Pinto M., Mele J., Buffenstein R. Successful aging and sustained good health in the naked mole rat: a long-lived mammalian model for biogerontology and biomedical research // ILAR Journal. 2011; 52 (1): 41–53.
.
Маленькая трагедия
Тем не менее при большом желании программу в процессах старения действительно можно найти – если искать не в генах, а уровнем выше, в эпигенетике. ДНК в наших клетках день за днем покрывается новыми эпигенетическими маркерами – метильными метками, и клетки постепенно и необратимо теряют доступ к собственной генетической информации.
С точки зрения теории "тела на выброс", все части тела (сомы) обречены на смерть, кроме клеток зародышевой линии, то есть половых. Но если присмотреться внимательнее, то сома оказывается неоднородной. Стволовые клетки долго сохраняются в полудетском состоянии, не старея, и в этом смысле их можно считать [610] Rando T. A. Stem cells, ageing and the quest for immortality // Nature. 2006 Jun; 441: 1080–1086.
непосредственным представительством зародышевой линии в соме. Но с течением времени в этих клетках включается программа – не смерти, но дифференцировки, что в некотором роде одно и то же. Получая профессию, потомки стволовых клеток прощаются с детством и бессмертием, впереди у них – долгая служба, а потом – в зависимости от обстоятельств – превращение в опухоль, старение или апоптоз. Программа, которая стоит за этими превращениями, – это фактически программа развития, и работа ее в конечном счете приводит к смерти.
Красивым подтверждением этому соображению является эксперимент [611] Lui G.-H. et al. Recapitulation of premature ageing with iPSCs from Hutchinson – Gilford progeria syndrome // Nature. 2011 Feb; 472: 221–225.
со стволовыми клетками, полученными от пациентов с детской прогерией. Эмбриональные стволовые клетки, которые находятся в самом начале пути и ближе прочих к зародышевой линии, не проявляют симптомов болезни. Они не производят мутантный ламин А, а он, в свою очередь, не нарушает структуру ядра, и эпигенетически такие клетки не старше, чем эмбриональные клетки здоровых людей. И только после начала дифференцировки клетка приобретает все положенные симптомы, начиная ускоренно стареть.
Мы не очень много знаем о том, как именно реализуется эта программа. Каждая клетка реагирует на набор сигналов, который приходит из ниши: от соседей, внеклеточного матрикса и из крови. В ответ на них, как правило, начинают работать факторы транскрипции, которые включают работу одних генов и выключают – других. Вслед за факторами транскрипции в игру включаются белки ремоделирования хроматина – те, что навешивают на ДНК и гистоны химические группы (эпигенетические метки), заставляя участки цепи скручиваться и раскручиваться. Так постепенно клетка теряет доступ к части своей информации и из стволовой превращается в дифференцированную.
Читать дальшеИнтервал:
Закладка:










