Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться
- Название:Против часовой стрелки. Что такое старение и как с ним бороться
- Автор:
- Жанр:
- Издательство:Альпина нон-фикшн
- Год:2020
- Город:Москва
- ISBN:978-5-0013-9314-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться краткое содержание
В своей книге биолог и научный журналист Полина Лосева выступает в роли адвоката современной науки о старении и рассказывает о том, чем сегодня занимаются геронтологи и как правильно интерпретировать полученные ими результаты. Кто виноват в том, что мы стареем? Что может стать нашей защитой от старости: теломераза или антиоксиданты, гормоны или диеты? Биологи пока не пришли к единому ответу на эти вопросы, и читателю, если он решится перейти от размышлений к действиям, предстоит сделать собственный выбор.
Эта книга станет путеводителем по современным теориям старения не только для биологов, но и для всех, кому интересно, как помочь своему телу вести неравную борьбу со временем.
Против часовой стрелки. Что такое старение и как с ним бороться - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Непосредственно механизм запрограммированного старения предложил [570] Skulachev V. P. Aging is a specific biological function rather than the result of a disorder in complex living systems: biochemical evidence in support of Weismann's hypothesis // Biochemistry (Moscow). 1997 Nov; 62 (11): 1191–1195.
в 1997 году Владимир Скулачев, специалист в области клеточного дыхания и один из создателей биоэнергетики, научной дисциплины, которая занимается обменом энергии в клетке. Скулачев обратил внимание на то, что у одноклеточных организмов – в частности, дрожжей – тоже встречается запрограммированная смерть, а механизмы ее схожи с апоптозом, клеточным самоубийством в организме млекопитающих. В обоих процессах участвуют белок р53, а также антиоксиданты и шапероны (белки – упаковщики белков). Поэтому Скулачев предложил считать гибель одноклеточных дрожжей и гибель отдельных клеток в многоклеточных организмах единым явлением и назвал его феноптозом .
Когда феноптоз не работает, клетка может справиться с поломками и свободными радикалами и остаться в живых. Когда феноптоз запущен, механизмы ремонта выключаются и начинают накапливаться те самые повреждения, которые приводят в конечном счете к старению или апоптозу клеток, а затем и к смерти организма. В этой теории находится место и онкологическим заболеваниям. Как только механизмы ремонта повреждений ослабевают, клетки перерождаются в опухолевые и убивают организм даже в отсутствие апоптоза. Поэтому Скулачев считает старение и рак следствиями одной программы и называет рак быстрым феноптозом, а старение – медленным, постепенным.
Программа старения и смерти, по Скулачеву, – это проявление альтруизма [571] Longo V. D., Mitteldorf J., Skulachev V. P. Programmed and altruistic ageing // Nature Reviews Genetics. 2005 Nov; 6: 866–872.
. Слабые организмы уступают место своим сильным собратьям, которые несут более выигрышные в данных условиях мутации. Эту логику можно применить не только к одноклеточным организмам, но и к крупным животным. Скулачев приводит в пример тихоокеанского лосося, который умирает сразу после того, как размножился, и тем самым, вероятно, освобождает место для развития своих потомков, а своим телом подкармливает беспозвоночных, которые тоже впоследствии станут пищей для следующего поколения.
Чтобы доказать, что программа старения действительно существует, необходимо привести примеры [572] Skulachev M. V. & Skulachev V. P. New data on programmed aging – slow phenoptosis // Biochemistry (Moscow). 2014 Oct; 79: 977–993.
обратного – то есть случаи, в которых она не работает и старость не наступает. Если принять теорию феноптоза, то таких примеров должно быть немало: ведь механизмы клеточного ремонта очень разнообразны, и заставить их работать бесперебойно можно множеством способов. Первым в списке примеров у Скулачева значится, конечно, голый землекоп, чьи клетки гораздо более устойчивы [573] Zhao Y. Naked mole rats can undergo developmental, oncogene-induced and DNA damage-induced cellular senescence // PNAS. 2018 Feb; 115 (8): 1801–1806.
к апоптозу, чем клетки других грызунов или человека, вероятно, благодаря поддержке длинных нитей гиалуроновой кислоты в межклеточном веществе. Вторыми следуют летучие мыши, которые, судя по всему, "сломали программу" ближе к корню и постоянно производят антиоксиданты. Что характерно, ни землекопы, ни летучие мыши, ни другие животные, которых относят к пренебрежимо стареющим, практически не болеют раком – и это подтверждает идею Скулачева о том, что рак и старение – явления одного рода.
Наконец, если программа существует, то ее можно выключить искусственно. Например, самцы австралийской бурой сумчатой мыши, как и лососи, погибают вскоре после спаривания. Оказалось [574] Bradley A. J., McDonald I. R., Lee A. K. Stress and mortality in a small marsupial ( Antechinus stuartii , Macleay) // General and Comparative Endocrinology. 1980 Feb; 40 (2): 188–200.
, что для того, чтобы вызвать у них скорую смерть, достаточно феромонов самки, а если кастрировать или изолировать самцов, то можно продлить им жизнь до уровня самок. Того же эффекта можно достичь и посредством манипуляций с генами: выключения одного-единственного гена бывает достаточно, чтобы продлить жизнь дрозофилы или нематоды C. elegans в 4–10 раз. С позвоночными, правда, такого эффекта достичь не удается – даже мыши, на которых уже перепробовали все, пока дольше четырех лет не живут.
Гадание на генах
Что же касается людей, то у них признаков программы старения еще меньше, чем у экспериментальных животных. Мы не умираем после размножения в одночасье, нет среди нас и долгоживущих "мутантов". Тем не менее сторонники теории запрограммированного старения не теряют надежды и продолжают поиски программы в наших генах.
С людьми в этом смысле все куда сложнее, чем с животными. Нельзя просто взять человека, отключить у него какой-нибудь ген и посмотреть, будет он жить дольше или нет. Нельзя скрещивать людей избирательно, чтобы получить у их детей интересующую ученых комбинацию генов. Поэтому приходится рассчитывать на то, что на земном шаре естественным путем уже скопилось достаточно разных генетических комбинаций, чтобы найти среди них какую-нибудь закономерность.
Основной метод, который для этого используют сейчас, – это полногеномный поиск ассоциаций (genome-wide association studies, GWAS). Ученые собирают последовательность геномов разных людей, а затем ищут связь между продолжительностью их жизни и отличиями в последовательности отдельных генов. Иными словами, пытаются построить модель, которая позволила бы предсказать срок жизни человека на основе тех вариантов генов, которые он несет в своих клетках.
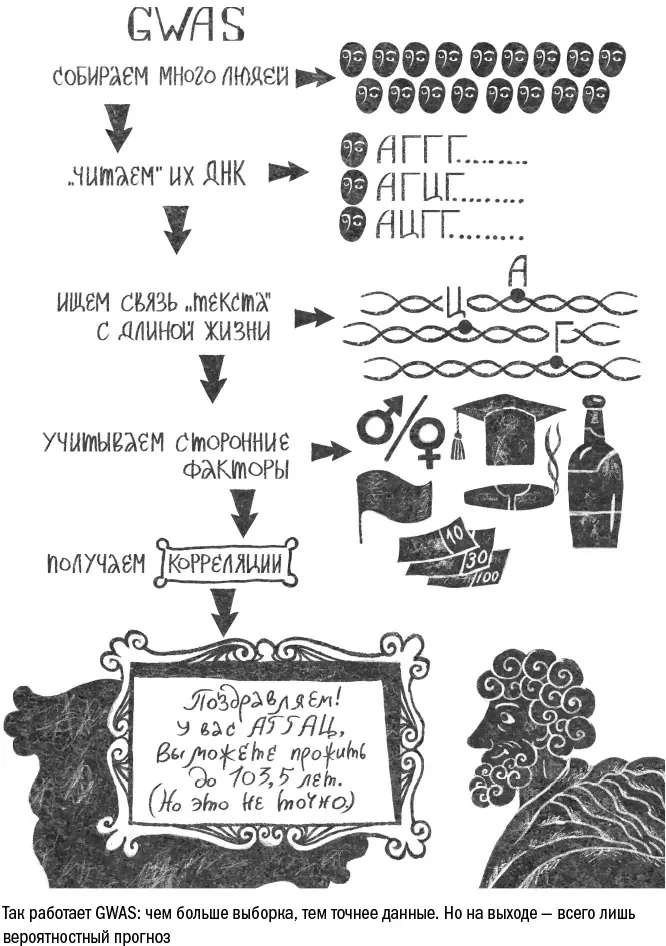
Для этого нужна большая выборка – в тысячи, а лучше сотни тысяч людей. За ней ученые обычно обращаются в биобанки – это базы данных, которые составлены по результатам многолетних исследований. Обычно такие исследования преследуют совсем другую цель – например, соотнести образ жизни с риском развития болезней, – но заодно собирают у участников множество анализов, включая генетические. Поэтому в каждом банке можно найти информацию не только о продолжительности жизни людей и их генотипе, но и о множестве деталей их биографии. Но поскольку действительно больших банков не так много и собирают их в основном в развитых странах, то результаты, которые ученые с их помощью получают, несколько перекошены – например, мы уже немало знаем о генах, которые связаны с долгой жизнью у британцев и исландцев, а вот у народов Азии и Африки закономерности могут оказаться совсем другими.
Тем не менее таких исследований уже было немало, и на их основе можно сделать два важных вывода. Первый – оптимистичный: долголетие определенно наследуется. Это, конечно же, не новость: давно известно, что существуют целые семьи долгожителей – в тех же "голубых зонах". Теперь этому есть и официальные подтверждения: у потомков долгожителей, например, на 62 % ниже риск смерти [575] Terry D. F. et al. Lower all‐cause, cardiovascular, and cancer mortality in centenarians' offspring // Journal of the American Geriatrics Society. 2004 Nov; 52 (12): 2074–2076.
от всех причин, чем у контрольной группы того же года рождения, на 71 % ниже риск смерти от опухолей и на 85 % – от болезней сердца.
Интервал:
Закладка:










