Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться
- Название:Против часовой стрелки. Что такое старение и как с ним бороться
- Автор:
- Жанр:
- Издательство:Альпина нон-фикшн
- Год:2020
- Город:Москва
- ISBN:978-5-0013-9314-6
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Полина Лосева - Против часовой стрелки. Что такое старение и как с ним бороться краткое содержание
В своей книге биолог и научный журналист Полина Лосева выступает в роли адвоката современной науки о старении и рассказывает о том, чем сегодня занимаются геронтологи и как правильно интерпретировать полученные ими результаты. Кто виноват в том, что мы стареем? Что может стать нашей защитой от старости: теломераза или антиоксиданты, гормоны или диеты? Биологи пока не пришли к единому ответу на эти вопросы, и читателю, если он решится перейти от размышлений к действиям, предстоит сделать собственный выбор.
Эта книга станет путеводителем по современным теориям старения не только для биологов, но и для всех, кому интересно, как помочь своему телу вести неравную борьбу со временем.
Против часовой стрелки. Что такое старение и как с ним бороться - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
С этой программой умеют работать, например, пчелы. Рассказывая о неравенстве по части продолжительности жизни, которое царит в пчелином улье, я упоминала, что оно поддерживается за счет еды. Рабочие пчелы питаются в основном пыльцой, а царице достается маточное молочко. Оказалось, что в нем содержится вещество ройалактин, которое подавляет активность метилтрансферазы – фермента, который навешивает эпигенетические метки на ДНК. Таким образом, царицы дольше остаются молодыми, чем рабочие пчелы.
Люди же научились эту программу не только выключать, но даже поворачивать вспять. В 2006 году японские ученые Шинья Яманака и Казутоши Такахаши придумали [612] Takahashi K., Yamanaka S. Induction of pluripotent stem cells from mouse embryonic and adult fibroblast cultures by defined factors // Cell. 2006 Aug; 126 (4): 663–676.
способ репрограммировать клетки, то есть возвращать их из дифференцированного состояния обратно в стволовое. Для этого необходимо добавить в клетку четыре белка (или запустить работу соответствующих им генов): Oct3 / 4, Klf-2, Sox-2 и c-Myc. Под действием этого "коктейля Яманаки" ДНК в ядре клетки перестраивается: частично скручивается, частично разворачивается. В результате всякая, даже терминально дифференцированная, клетка превращается в эмбриональную стволовую, то есть возвращается на ту стадию, когда она способна произвести любые клеточные типы, из которых состоит тело взрослого организма. Такие стволовые клетки называют индуцированными плюрипотентными – дословно это означает, что в них искусственным образом запустили плюрипотентность, способность давать начало множеству производных.
В 2012 году ученые получили за это открытие Нобелевскую премию, а исследователи по всему миру начали придумывать, где бы еще его можно было применить. Первая мысль, которая приходит в голову, – репрограммировать клетки взрослого человека, чтобы вырастить ему какой-нибудь запасной орган или ткань. Это действительно возможно, и в некоторых странах уже идут испытания таких тканей – например, роговицы или предшественников нервных клеток для лечения болезни Паркинсона.
Но каждый орган или ткань в отдельности выращивать довольно долго и дорого, даже если не брать во внимание медицинские риски, которые при этом возникают, – например, риск отторжения трансплантата. Поэтому для борьбы со старением было бы удобнее научиться репрограммировать клетки in vivo , то есть внутри живого организма. Постепенно оказалось, что для этого есть все предпосылки: репрограммированию поддаются любые клетки человека, в том числе [613] Lapasset L. et al. Rejuvenating senescent and centenarian human cells by reprogramming through the pluripotent state // Genes & Development. 2011; 25: 2248–2253.
сенесцентные клетки и клетки, взятые у долгожителей. После обработки факторами Яманаки к этим клеткам возвращается молодость – и по длине теломер, и по набору работающих генов, и по часам метилирования они начинают напоминать клетки зародыша.
Но если омолаживать клетки непрерывно, то взрослые клетки будут превращаться в эмбриональные и образовывать опухоли. Именно это произошло с мышами, у которых ученые усилили экспрессию факторов Яманаки: в их организме [614] Abad M. et al. Reprogramming in vivo produces teratomas and iPS cells with totipotency features // Nature. 2013 Sep; 502: 340–345.
появились настоящие плюрипотентные клетки и выросли тератомы – опухоли из множества разных типов клеток. Тем не менее так удалось показать, что репрограммирование in vivo тоже возможно.
Чтобы омоложение не заканчивалось ростом опухолей, нужно как-то научиться дозировать работу факторов Яманаки: тогда клетки не будут превращаться сразу в зародышевые, а просто немного "откатят" свою программу дифференцировки назад. Для этого ученые создали специальную линию мышей, у которых под действием определенного лекарства можно запустить в клетках работу четырех факторов Яманаки, а лишив их лекарства – ее выключить. Оказалось [615] Ocampo A. et al. In vivo amelioration of age-associated hallmarks by partial reprogramming // Cell. 2016 Dec; 167 (7): 1719–1733. E12.
, что если включать четыре гена небольшими порциями, на два – четыре дня, а потом делать перерыв, то этого хватает, чтобы клетки потеряли признаки сенесцентных и помолодели эпигенетически, а вот потерять свою специализацию и вернуться в зародышевое состояние они не успевают.
После однократной "стимуляции молодости" признаки старости появляются снова. Но если действовать медленно и упорно, повторяя цикл "два дня омоложения – пять дней отдыха" десятки раз, то клетки не возвращаются в сенесцентное состояние. Эту методику ученые для начала проверили на ускоренно стареющих мышах – которые послужили моделью детской прогерии человека – и увеличили таким образом срок их жизни с 22 недель до 29. Потом попробовали то же самое на обычных мышах: им краткое репрограммирование позволило восстановить поджелудочную железу и мышцы после травмы.
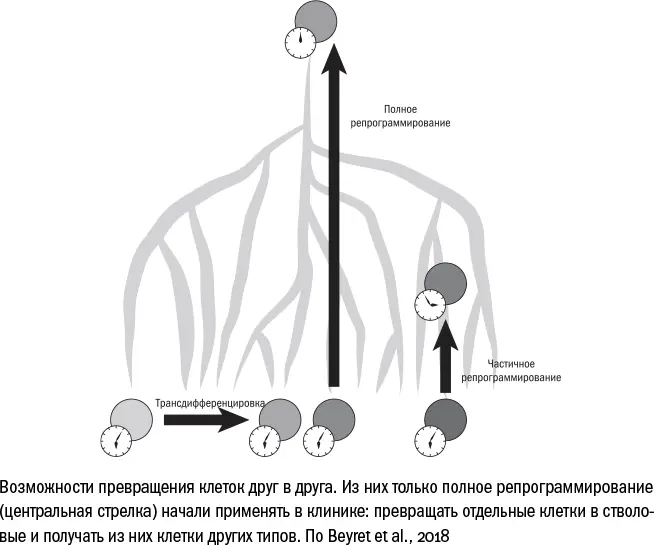
История с репрограммированием целого организма находится еще только в начале своего пути. Данных пока немного, и мы до сих пор не знаем [616] Beyret E. et al. Elixir of Life // Circulation Research. 2018 Jan; 122: 128–141.
, удастся ли таким образом продлить жизнь здоровым животным. Кроме того, в экспериментах использовали специально выведенные линии мышей: они генетически модифицированы, чтобы запускать работу факторов Яманаки в ответ на лекарство. Едва ли этот метод напрямую можно будет применить к людям. Значит, придется придумать какие-то методы доставки "коктейля Яманаки" во взрослый организм.
Пока наиболее реалистичными выглядят методы локального репрограммирования [617] Kurita M. et al. In vivo reprogramming of wound-resident cells generates skin epithelial tissue // Nature. 2018 Sep; 561: 243–247.
, которые тоже постепенно начинают пробовать на мышах. Например, в эксперименте 2018 года на спине у мышей создавали незаживающую рану (для этого края раны отделяли от центра специальным стеклом), а внутрь нее вводили обезвреженные вирусы со специальным набором факторов транскрипции. Вирусы проникали в клетки соединительнотканного слоя кожи и с помощью факторов транскрипции превращали их в клетки поверхностного слоя кожи. Подобным образом удалось перепрограммировать клетки из одного типа в другой и зарастить раневую поверхность. Можно предположить, что таким же способом однажды удастся восстановить и поврежденные органы человека.
Кстати, клетки голого землекопа, в отличие от клеток мыши или человека, к репрограммированию устойчивы [618] Tan L. et al. Naked mole rat cells have a stable epigenome that resists iPSC reprogramming // Stem Cell Reports. 2017 Nov; 9 (5): 1721–1734.
. В них гораздо больше метильных меток на гистонах, которые усиливают скручивание ДНК, поэтому развернуть ее обратно "коктейлю Яманаки" не под силу. Вероятно, это еще одно следствие механизмов, с помощью которых голый землекоп защищается от рака. Но, так или иначе, это лишает нас возможности попробовать продлить его жизнь еще больше. Получается своеобразный парадокс: животное, которое служит опорой теории запрограммированного старения, не способно обратить вспять единственную программу – развития и дифференцировки, – существование которой убедительно доказано.
Интервал:
Закладка:










