Михаил Ермолаев - Биологическая химия
- Название:Биологическая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:1974
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Ермолаев - Биологическая химия краткое содержание
В учебнике нашли отражение последние научные данные о ферментах, белках, гормонах, обмене веществ и энергии и т. д. Особое внимание обращено на значение и использование данных биохимии в медицине, в связи с чем расширены разделы, посвященные патологии разных видов обменов и их исследованиям в клинике Включены материалы по наследственным заболеваниям, связанным с нарушением синтеза белка и ферментов.
Учебник написан по программе, утвержденной Министерством здраво" хранения СССР, и предназначен для учащихся фельдшерско-лаборантских отделениях медицинских училищ.
Биологическая химия - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
На основании различного распределения трансаминаз в сердце и печени установлено, что при инфаркте миокарда в сыворотке преимущественно повышается активность ГЩУТ, а при заболеваниях печени — ГПТ.
Декарбоксилирование
Декарбоксилирование аминокислот заключается в отщеплении от аминокислот СО 2с образованием при этом аминов^ и катализируется ферментами декарбоксилазами. Процесс происходит по следующей схеме:
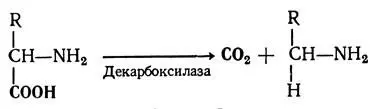
Таким путем из триптофана образуется гриптамин и серотонин (5-оксигриптамин), из гистидина — гистамин, из глютаминовой кислоты — γ-аминомасляная кислота. Образующиеся при этом амины оказывают на организм мощный биологический эффект, в связи с чем их называют биогенными аминами .
Так, введение гистамина вызывает:
1. расширение капилляров и соответственно повышение их проницаемости;
2. сужение крупных сосудов;
3. сокращение гладкой мускулатуры различных органов и тканей;
4. возбуждение секреции соляной кислоты в желудке.
Серотонин способствует повышению кровяного, давления и сужению бронхов. Противоречиво действие серотонина на центральную нервную систему, когда малые количества подавляют, а более значительные количества, наоборот, стимулируют центральную нервную систему.
γ-Аминомасляная кислота является медиатором центральной нервной системы. В организме большие количества гистамина и серотонина находятся в неактивной, связанной форме в различных тканях. Биологическое действие проявляют только свободные формы этих веществ. Распад гистамина и серотонина и других биогенных аминов происходит при посредстве неспецифической моноаминоксидазы.
Конечные продукты распада аминокислот
В результате различных превращений аминокислот в тканях организма образуются аммиак, углекислый газ и вода. Углекислый газ частично выводится из организма, а оставшаяся часть используется для синтетических процессов, например для синтеза жирных кислот, пуриновых оснований и др.
Аммиак образуется в организме при дезаминировании аминокислот, при распаде некоторых веществ, таких, как пуриновые и пиримидиновые основания, глютамин и др. Например, в почках аммиак выделяется при распаде глютамина.
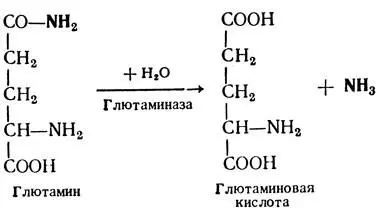
Аммиак для организма является очень сильным токсическим веществом. Например, повышение его концентрации в крови только на 5% приводит к гибели кроликов. Поэтому организм в ходе эволюции выработал различные эффективные механизмы его обезвреживания. К основным из них относятся: образование глютамина, восстановительное аминирование, нейтрализация кислот, синтез мочевины.
Образование глютаминаимеет важное значение для организма. Это связано с тем, что синтез глютамина в основном происходит в местах непосредственного образования аммиака, например в печени и мозге, где обнаружена активная глютаминсинтетаза — фермент, катализирующий этот процесс. В результате этого предотвращается проявление токсического действия аммиака. Обезвреженный таким путем NH 3может быть использован организмом в качестве источника азота, например, для синтеза пуриновых и пиримидиновых оснований, мукополисахаридов (глюкозамин). Это характеризует взаимосвязь белкового обмена с обменом нуклеиновых кислот и углеводов. Глютамин выступает в этих процессах в качестве транспортной формы аммиака.
Восстановительное аминированиепредставляет собой процесс, обратный дезаминированию. Он обеспечивает связывание аммиака кетокислотами с образованием соответствующих им аминокислот. В организме обнаружена активная ферментная система, которая катализирует восстановительное аминирование α-кетоглютаровой кислоты с образованием глютаминовой.
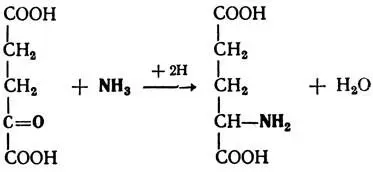
Нейтрализация неорганических и органических кислотаммиаком с образованием аммонийных солей является процессом обезвреживания аммиака в почках.
Синтез мочевины
Синтез мочевиныслужит основным путем детоксикации аммиака у млекопитающих и главной формой выделения белкового азота из организма. Из общего числа азотистых веществ в моче на долю азота мочевины приходится от 80 до 85%. Впервые принципиальная схема синтеза мочевины была предложена М. В. Ненцким. Ему удалось доказать, что синтез мочевины происходит из двух молекул аммиака и одной молекулы углекислого газа:
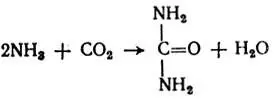
В специальных опытах И. В. Залеский и С. С. Салазкин в лаборатории И. П. Павлова установили, что если кровь воротной вены направить не в печень, а в нижнюю полую вену, т. е. миновать печень, то наступает резкое увеличение содержания аммиака в крови и отравление животного, нередко заканчивающееся его гибелью. Был сделан вывод, что печень является органом, где происходит обезвреживание аммиака.
Работами Кребса, Эмбдена, Клементи, Ратнера и других авторов было выяснено участие в этом процессе других веществ и ферментов, катализирующих реакции синтеза мочевины.
В современном представлении синтез мочевины изображен на схеме 4.
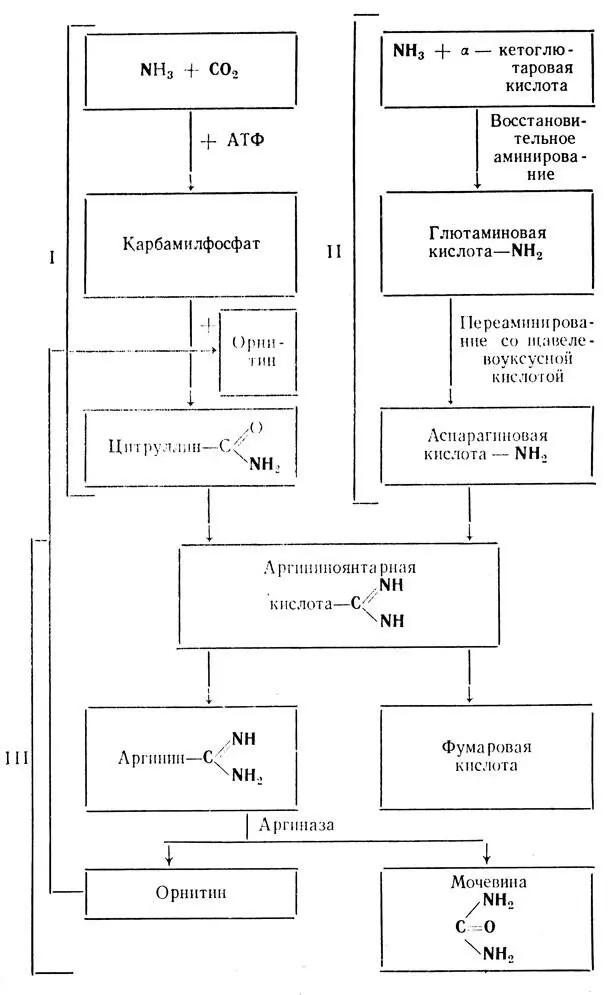
Схема 4
При детальном изучении синтез мочевины можно условно разделить на 3 этапа. На первых двух происходит связывание двух молекул аммиака в безвредные для организма соединения, а на третьем фактически происходит образование мочевины.
I этап.Молекула аммиака и углекислого газа за счет энергии, выделяемой при распаде АТФ, синтезируется в карбамилфосфат, который, соединяясь с орнитином (неприродная аминокислота), образует цитруллин.
Таким образом, в цитруллине зафиксированы одна молекула аммиака и СО 2.
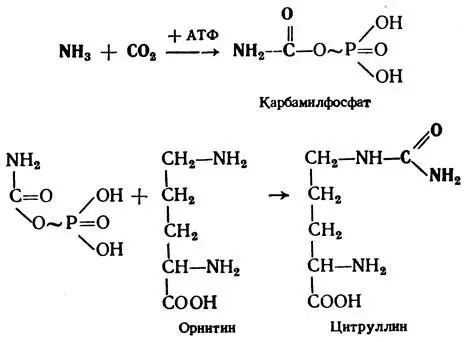
II этап.Происходит связывание еще одной молекулы аммиака в глютаминовой кислоте путем восстановительного аминирования с α-кетоглютаровой кислотой. Глютаминовая кислота передает зафиксированную молекулу аммиака в виде NН 2-группы на щавелевоуксусную кислоту, которая превращается в аспарагиновую кислоту (процесс переаминирования).
Читать дальшеИнтервал:
Закладка:






