Валерий Крылов - Каталитический риформинг бензинов. Теория и практика
- Название:Каталитический риформинг бензинов. Теория и практика
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:2021
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Валерий Крылов - Каталитический риформинг бензинов. Теория и практика краткое содержание
В книге представлен анализ теоретических и практических положений технологии процесса каталитического риформинга бензиновых фракций. Изложен опыт и приведены лучшие практики эксплуатации современных установок риформинга.
Книга предназначена для инженерно-технических работников нефтеперерабатывающих заводов, проектных организаций, преподавателей и студентов вузов.
Каталитический риформинг бензинов. Теория и практика - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Изомеризация н-парафиновых углеводородов включает в себя дегидрирование на металлических центрах с образованием олефинов нормального строения, изомеризацию полученных олефинов на кислотных центрах с образованием олефинов изостроения и гидрирование на металлических центрах до изопарафина. На примере этого превращения становятся понятными преимущества бифункционального катализатора.
Промежуточным соединением в реакции скелетной изомеризации является карбениевый ион, имеющий структуру с трехкоординированным атомом углерода.
В случае олефина образование карбениевого иона происходит достаточно легко при атаке протона, предоставляемого кислотным центром Бренстеда, на π-связь. При этом π-связь разрывается и образуется новая С–Н-связь.
Если же исходным углеводородом является алкан, то
образование карбениевого иона включает атаку протона на
С–Н-связь. При этом вначале образуется промежуточный карбониевый ион, представляющий катион с пятикоординированным атомом углерода. Например, при протонировании 2-метилпентана образуется карбониевый ион (рис. 17, б ). Распад этого катиона приводит к образованию карбениевого иона и молекулы Н 2(см. рис. 17, а ).
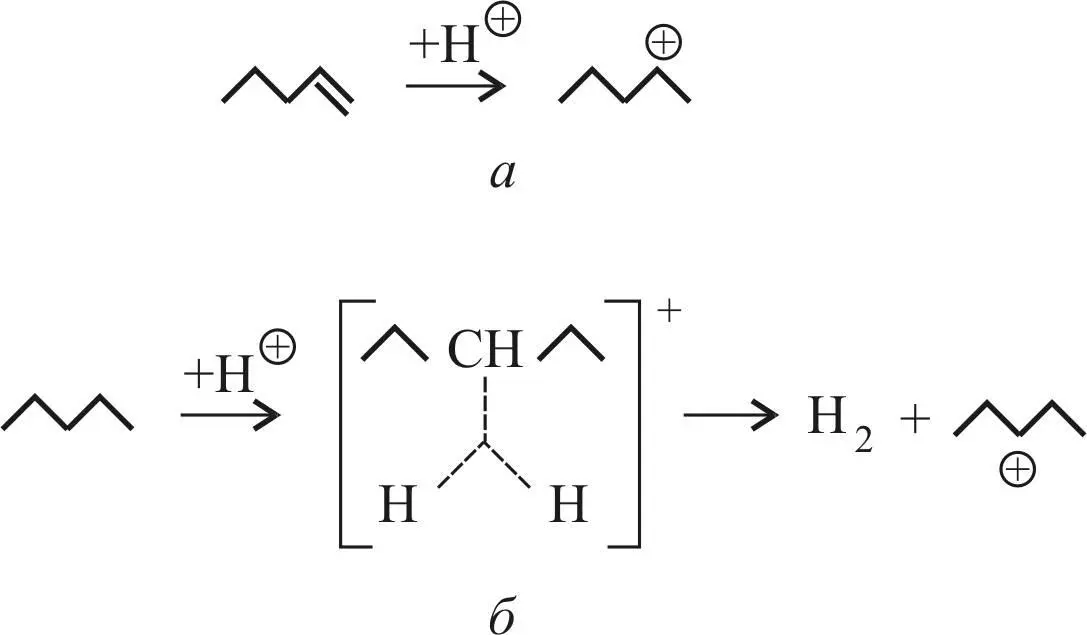
Рис. 17. Схема образования:
а – карбениевого иона; б – карбониевого иона
В этом случае разрывается более прочная С–Н-связь.
Значительная разница в энергиях связи (394–239 = 155 кДж/моль) делает возможным образование карбениевого иона из алкана лишь при использовании твердых суперкислот, например, Н-морденитов с силикатным модулем около 20, в условиях же платформинга подобный механизм не реализуется.
Глава 9. Катализ на
d
-металлах
Природа каталитических свойств d -металлов. Связь с координационной ненасыщенностью поверхностных атомов металлов.
Донорно-акцепторная и дативная связи в металлорганических комплексах. Модель Дьюра – Чата – Дункансона.
Механизм образования связей на примере молекулы СО.
Ослабление связей в молекуле СО как результат образования донорно-акцепторной и дативной связи.
Как образуются d -зоны в металлических катализаторах.
Почему происходит химическая адсорбция.
Активация молекул как результат хемосорбции.
Принцип Сабатье и вулканообразные кривые Баландина.
Почему платина является базовым элементом катализаторов риформинга.
Почему реакции дегидрирования являются быстрыми реакциями, а реакции гидрогенолиза медленными: каталитический эффект платины
Каталитическая активность d -металлов обусловлена координационной ненасыщенностью атомов, образующих поверхностные грани металлических частиц.
Координационное число (КЧ) платины, формирующей гранецентрированную кубическую решетку (ГЦК), равно 12.
КЧ для поверхностных атомов зависят от типа поверхности и составляют 9 для граней (111), 8 для (100) и 7 для (110).
Атомы на ступенях и изломах, ребрах и углах частиц имеют еще меньшие КЧ – от 7 до 5 [54].
Вывод атома из объема металла на поверхность является сильно эндотермическим процессом, связанным с разрывом связей с соседними атомами.
Энергия, необходимая для образования поверхностного атома, прямо пропорциональна энергии когезии металла и координационной ненасыщенности поверхностного атома.
Уменьшение размера частицы также приводит к увеличению поверхностной энергии за счет увеличения доли поверхностных атомов.
Переход системы в более устойчивое состояние с меньшей энергией Гиббса достигается путем коалесценции частиц при повышенных температурах или за счет адсорбции молекул окружающей среды. Из двух видов адсорбции, физической и химической, последняя имеет ключевое значение для гетерогенного катализа, так как связана с активацией молекулы, обусловленной изменениями ее электронной структуры при адсорбции на поверхности твердого тела.
В основе современного понимания механизма химической адсорбции и катализа на d -металлах лежат идеи о координационно-донорной и дативной связях и d -зоне, которые были заимствованы из металлорганической химии и физики твердого тела соответственно.
Дьюар в 1951 году предложил модель образования соли Цейзе и ее палладиевого аналога, комплекса Караша, представляющих собой комплексы этилена и металла (рис. 18) [37].
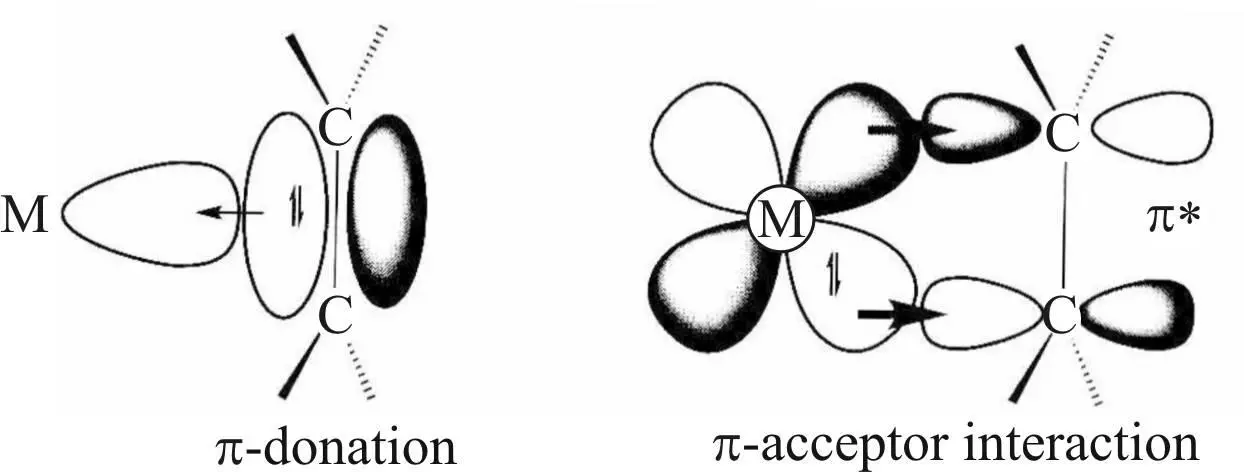
Рис. 18. Структура комплексов Pt(Pd) c этиленом
В соответствии с этой моделью, в доработанном виде носящей название модели Дьюара – Чата – Дункансона, в образовании комплекса принимают участие два типа связей: донорно-акцепторная связь, образуемая за счет передачи электронной плотности π-связи молекулы этилена на вакантную d -орбиталь атома платины, и дативная связь, которая возникает за счет перекрытия заполненной d -орбитали атома металла с разрыхляющей орбиталью молекулы этилена. Заметим, что обе связи являются примером донорно-акцепторного взаимодействия, так что выделение дативной связи сделано для удобства, это указание на то, что донором в этом случае является металл.
Атомными орбиталями, удовлетворяющими этому требованию, являются dz 2– и dxz -орбитали переходного металла.
Ниже представлены схемы образования донорно-акцепторной и дативной связей d -металла и молекулы этилена (рис. 19). Донорно-акцепторная связь образуется при перекрывании π-МО этилена с dz 2-AO металла. В образовании дативной связи участвуют разрыхляющая π*-МО этилена и dxy -АО металла.
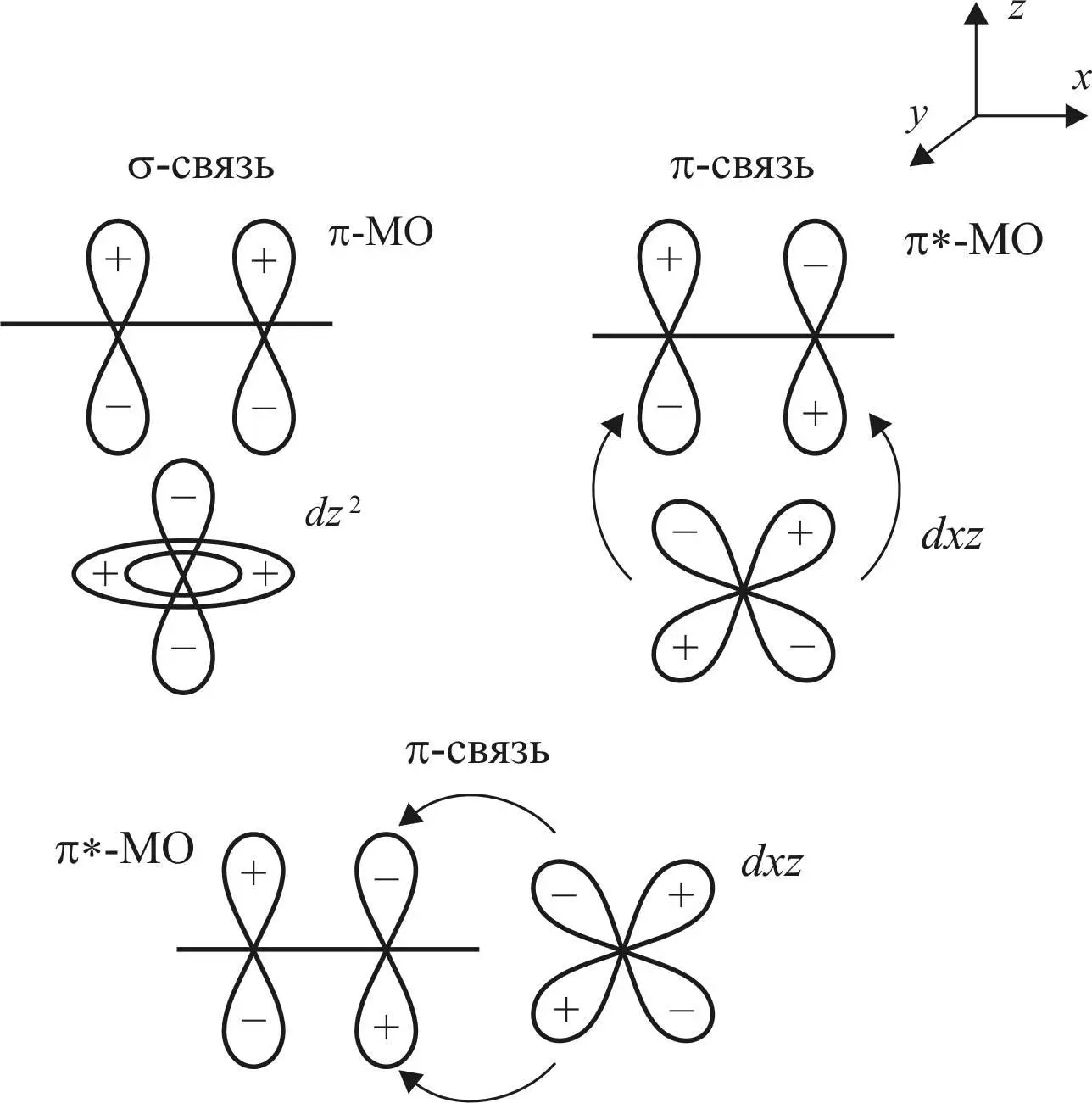
Рис. 19. Схема образования – и π-связей:
стрелками показаны направления смещения электронной плотности
Образование донорно-акцепторной связи осуществляется по σ-типу, а дативной связи – по π-типу.
Для образования дативной связи возможны два варианта перекрывания орбиталей.
Из-за небольших стерических затруднений, возникающих при боковом перекрывании, в рассмотренных комплексах реализуется схема с расположением иона металла над или под плоскостью, в которой находятся sp 2-орбитали молекулы этилена.
При отсутствии таких ограничений может реализовываться схема с боковым перекрыванием, например, при образовании связи с молекулой СО, где такому перекрыванию способствует также несимметричное распределение электронной плотности в лепестках разрыхляющей орбитали, связанное с поляризацией связи.
Читать дальшеИнтервал:
Закладка:









