Е. Бессолицына - Биохимия метаболизма. Учебное пособие
- Название:Биохимия метаболизма. Учебное пособие
- Автор:
- Жанр:
- Издательство:Литагент Ридеро
- Год:неизвестен
- ISBN:9785448336638
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Е. Бессолицына - Биохимия метаболизма. Учебное пособие краткое содержание
Биохимия метаболизма. Учебное пособие - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Реакция образования ацетил-СоА, катализируемая пируватдегидрогеназным комплексом, регулируется в животных тканях при помощи ковалентной модификации этого комплекса. Когда концентрация АТФ в митохондриях относительно велика и когда ацетил-СоА, а также промежуточные продукты цикла Кребса имеются в достаточном количестве, обеспечивающем удовлетворение энергетических нужд клетки, дальнейшее образование ацетил-СоА приостанавливается. В этих условиях, которые служат сигналом для такой приостановки, АТФ является положительным модулятором, активирующим вспомогательный фермент – киназу пируватдегидрогеназы.Этот фермент использует АТФ для фосфорилирования остатка серина в активном центре молекулы пируватдегидрогеназы, в результате чего образуется неактивная форма фермента – фосфопируватдегидрогеназа.
Если, однако, потребность в АТФ возрастает и уровень АТФ соответственно снижается, то неактивная, фосфорилированная, форма пируватдегидрогеназы может быть вновь активирована. Это происходит в результате гидролитического отщепления от молекулы пируватдегидрогеназы ингибирующей фосфатной группы. Катализирует эту реакцию другой фермент – фосфатаза фосфопируватдегидрогеназы.Стимулирующее действие на этот фермент оказывает повышение концентрации ионов Са 2+, играющих роль важного метаболического посредника; концентрация ионов Са 2+увеличивается всякий раз, когда возникает потребность в АТФ.
Киназа пируватдегидрогеназы и фосфатаза фосфопируватдегидрогеназы присутствуют в пируватдегидрогеназном комплексе. Этот комплекс, следовательно, представляет собой очень сложную, независимую и саморегулирующуюся систему. Пируватдегидрогеназный комплекс регулируется также путем аллостерической модуляции. Сильное ингибирующее действие оказывают на него (помимо АТФ) ацетил-СоА и NADH, которые являются продуктами пируватдегидрогеназной реакции и в то же время играют роль аллостерических ингибиторов этой системы. Аллостерическое ингибирование окисления пирувата резко усиливается в присутствии высокомолекулярных жирных кислот; ниже будет показано, что жирные кислоты тоже служат источником ацетил-СоА. Таким образом, каталитическая активность пируватдегидрогеназного комплекса выключается в тех случаях, когда в клетках имеется достаточно топлива в виде жирных кислот и ацетил-СоА или когда в них повышаются концентрация АТФ и отношение NADH/NAD +.
Цикл трикарбоновых кислот
Ацетил-СоА поступает в цикл трикарбоновых кислот, который является вторым этапом клеточного дыхания. Впервые предположение о существовании такого цикла для окисления пирувата в животных тканях было высказано в 1937 г. Гансом Кребсом. Эта идея родилась у него, когда он исследовал влияние анионов различных органических кислот на скорость поглощения кислорода суспензиями измельченных грудных мышц голубя, в которых происходило окисление пирувата. Грудные мышцы отличаются чрезвычайно высокой интенсивностью дыхания, что делает их особенно удобным объектом для изучения окислительной активности. Незадолго до описываемых работ Кребса Альберт Сент-Дьёрдьи в Венгрии обнаружил, что некоторые четырехуглеродные дикарбоновые органические кислоты, присутствующие в животных тканях (янтарная, фумаровая, яблочная и щавелевоуксусная), способны усиливать поглощение кислорода мышечной тканью. Кребс подтвердил это наблюдение и показал, что перечисленные органические кислоты стимулируют также окисление пирувата. Кроме того, он нашел, что окисление пирувата мышечной тканью стимулируется шестиуглеродными трикарбоновыми кислотами – лимонной, цис-аконитовой и изолимонной, а также пятиуглеродной α-кетоглутаровой кислотой. Испытаны были и некоторые другие встречающиеся в природе органические кислоты, но ни одна из них не обнаружила подобной активности. Обращал на себя внимание сам характер стимулирующего действия активных кислот: даже малого количества любой из них было достаточно для того, чтобы вызвать окисление во много раз большего количества пирувата.
Цикл трикарбоновых кислот выполняет несколько функций.
Во-первых, цикл трикарбоновых кислот представляет собою конечный общий путь для окисления топливных молекул. Большинство топливных молекул вступают в цикл в виде ацетил-СоА.
Во-вторых, образующиеся в реакциях цикла трикарбоновых кислот активные восстановительные эквиваленты, такие как NADH и FADH 2, затем поступают в третий этап – окислительное фосфорилирование, в результате которого образуется основная масса молекул АТФ. Именно поэтому цикл трикарбоновых кислот является одним из основных путей энергетического обмена.
В-третьих, цикл трикарбоновых кислот служит также источником строительных блоков для процессов биосинтеза.
Цикл трикарбоновых кислот осуществляется в митохондрии, где располагаются ферменты, катализирующие реакции этого цикла. Большая часть ферментов располагается в матриксе митохондрии. Исключение – α-кетоглутаратдегидрогеназа и сукцинатдегидрогеназа, располагающиеся во внутренней мембране митохондрии.
Несмотря на то, что реакции замкнуты в цикл, их можно подразделить на два этапа: окисление ацетил коА до СО 2и регенерация оксалоацетата (последовательность реакций цикла трикарбоновых кислот представлена на рисунке 8).
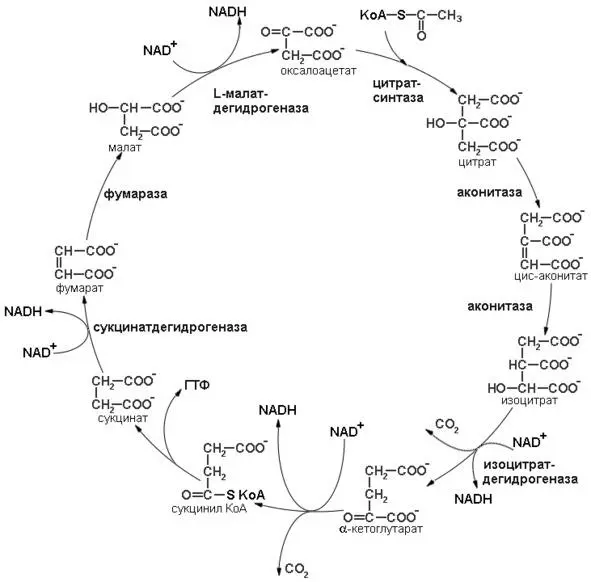
Рисунок 8: Схема реакций цикла трикарбоновых кислот.
Первая стадия окисления ацетил-СоА начинается с начальной реакции цикла. Начальная реакция – конденсация ацетил-СоА и оксалоацетата, приводящая к образованию цитрата, катализируется конденсирующим ферментом, цитратсинтазой,при этом происходит образование связи углерод-углерод между метильным углеродом ацетил-СоА и карбонильным углеродом оксалоацетата. За реакцией конденсации, приводящей к образованию цитрил-СоА, следует гидролиз тиоэфирной связи, сопровождающийся потерей большого количества свободной энергии в форме теплоты; это определяет протекание реакции слева направо до ее завершения. Превращение цитрата в изоцитрат катализируется аконитазой(аконитатгидратазой), содержащей ион железа в Fe 2+-состоянии. Ион железа является кофактором, обеспечивающим правильную организацию каталитического центра. Аконитаза относится классу лиаз, а не изомераз, как могло бы показаться на первый взгляд. Эта реакция осуществляется в две стадии: сначала происходит дегидратация с образованием цис-аконитата (часть его остается в комплексе с ферментом), а затем – гидратация и образование изоцитрата. Реакция ингибируется фторацетатом,который сначала превращается во фторацетил-СоА; последний конденсируется с оксалоацетатом, образуя фторцитрат. Непосредственным ингибитором аконитазы является фторцитрат; при ингибировании накапливается цитрат.
Читать дальшеИнтервал:
Закладка:










