Михаил Левицкий - Карнавал молекул. Химия необычная и забавная
- Название:Карнавал молекул. Химия необычная и забавная
- Автор:
- Жанр:
- Издательство:Литагент Альпина
- Год:2019
- Город:Москва
- ISBN:978-5-0013-9101-2
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Левицкий - Карнавал молекул. Химия необычная и забавная краткое содержание
В книге рассказано о некоторых драматичных, а, порой, забавных поворотах судьбы как самих открытий, так и их авторов. Кроме того, читатель потренируется в решении занятных задач, что особенно приятно, когда рядом помещена подсказка, а потом и сам ответ.
В отличие от учебника в книге нет последовательного изложения основ химии, поэтому ее можно читать, начиная с любой главы.
Карнавал молекул. Химия необычная и забавная - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Применяемые для этого катализаторы – нафтенат меди либо ее галогенид – малоэффективны и довольно быстро теряют активность. В поисках новых катализаторов ученые обратились к металлоорганосилоксанам – соединениям, содержащим группировки – RSi – O-M – О – RSi – O–. Они привлекательны тем, что позволяют вводить в их структуру различные атомы металлов, плавно регулируя атомное соотношение M/Si, кроме того, они растворимы в большинстве органических растворителей, что увеличивает диапазон их использования.
Металлоорганосилоксаны, содержащие фрагменты – SiR – O – M–, в роли катализаторов ранее не изучались в процессах такого типа, но они оправдали возлагаемые на них надежды: конверсия (степень превращения) симметричного продукта в несимметричный (в течение 1 часа) составила 72 %, что почти в четыре раза выше, чем на использованных прежде катализаторах.
Наиболее заметное отличие нового катализатора от изученных прежде – исключительно высокая стабильность каталитических свойств: многократное использование такого катализатора (6–10 раз) не приводит к заметному снижению его активности.
Галогенировать без элементарного галогена
Хлорсодержащие углеводороды служат исходными соединениями при получении самых разнообразных органических веществ, в связи с чем галогенирование входит в круг многотоннажных процессов органического синтеза, однако такие процессы экологически неблагоприятны из-за использования элементарного хлора.
Существуют иные пути получения хлоруглеводородов: например, обменное галогенирование CCl 4с алканами, когда алкан «забирает» хлор у хлорсодержащего соединения (рис. 3.37).
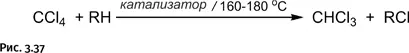
Взаимодействие пары реагентов декан С 10Н 12 – четыреххлористый углерод CCl 4катализируют различные комплексы меди, однако в процессе работы они быстро теряют активность. Медьсодержащий силоксан по каталитической активности заметно уступает комплексам меди (в 4–5 раз), но превосходит по стабильности каталитических свойств, его активность практически не снижается после пятикратного использования, в то время как эталонный катализатор полностью теряет работоспособность в течение одного цикла.
Подробное изучение процесса показало, что увеличение содержания катализатора не приводит к существенному возрастанию конверсии (превращение исходного соединения в конечный продукт). То же самое наблюдали в другом похожем процессе.
Если катализатор не ведет к селективности
В процессе обменного галогенирования хлор присоединяется к любому из атомов углерода в декане, в результате образуется смесь монохлорированных соединений (не затрагиваются практически лишь концевые СН 3-группы). Такая низкая селективность (избирательность) обычно не удовлетворяет химиков, частично проблему можно решить, изменив строение исходного реагента. Если вместо алкана взять алкен (углеводород с двойной связью), то положение двойной связи само укажет то место, куда должен присоединиться Cl и, соответственно, фрагмент CCl 3. Это было проверено с использованием октена C 6Н 13CН=CH 2(рис. 3.38).

Так же, как в предыдущих двух процессах, катализатор сохранял стабильность каталитических свойств при многократном использовании. Интересно, что вновь подтвердилось отмечавшееся явление: максимальная активность катализатора (определяемая как степень превращения, приходящаяся на один каталитический центр) наблюдается только при очень малом его содержании.
Явно прослеживалась закономерность, с которой необходимо было разобраться. Это нельзя было объяснить тем, что часть каталитических центров находилась в глубинных слоях катализатора и была недоступна для процесса. Объяснение получили при изучении особенностей строения самого катализатора, о чем речь пойдет ниже.
Обходной маневр
То, что заметная часть атомов меди оказывается «выключенной» из каталитического процесса, удалось объяснить с помощью магнитных измерений и спектральных исследований исходных металлоорганосилоксанов. Выяснилось, что значительная часть атомов металла связана в межцепные координационные кластеры. Металл стремится заполнить свою координационную сферу, привлекая атомы кислорода соседних фрагментов – Si – O – M– (координационные взаимодействия показаны пунктирными линиями на рис. 3.39).
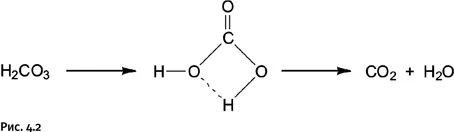
В результате атом Cu оказывается координационно-насыщенным и его взаимодействие с реагентом CCl 4затруднено. Как предотвратить образование межцепных кластеров? Можно, например, «укрыть» металл каким-либо лигандом, что, безусловно, затормозит межцепную координацию, но не поможет решить основную задачу – лиганд в свою очередь затруднит приближение реагента. Все же решение удалось найти, когда привлекли к участию органическую группу, связанную с кремнием. Жесткая и малоподвижная фенильная группа, обрамляющая кремний в исследованных металлоорганосилоксанах, не может препятствовать координационному взаимодействию атомов меди в соседних цепях. Если заменить фенильную группу Ph нонильной C 9H 19, то ситуация меняется (сетчатая поверхность на рис. 3.40 условно обозначает так называемые ван-дер-ваальсовы радиусы – ту часть пространства, которую реально занимает фрагмент молекулы).
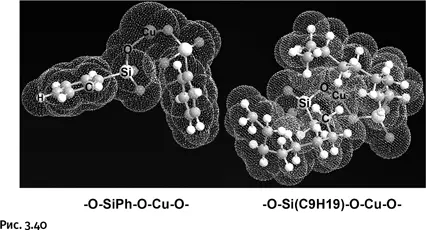
Объемистая алифатическая группа эффективно препятствует координационному взаимодействию атомов меди в соседних цепях, «окутывая» металлические центры, но в реакционной среде она обладает подвижностью и не препятствует приближению реагента ССl 4к каталитическому центру. Таким образом, четыреххлористый углерод может отодвинуть нонильную группу и приблизиться к каталитическому центру, но этого не может сделать атом меди в соседней цепи.
Результаты экспериментов оказались весьма убедительными: при каталитическом присоединении CCl 4к октену-1 активность медьсилоксанов, обрамленных нонильными группами, оказалась вдвое выше, чем у медьфенилсилоксанов.
Автор работ, о которых здесь было рассказано, – профессор В.В Смирнов (рис. 3.41), работавший на химическом факультет МГУ. Он любил повторять: «Найти катализатор – половина дела. Не менее важно научиться им управлять».

То живописное полотно, о котором мы говорили в самом начале этой главы, постоянно расширяется и дополняется, что не мешает нам смотреть с интересом на всю картину в целом, а также всматриваться в ее отдельные фрагменты, наблюдая за тем, как развивается замечательная область химии, именуемая катализом.
Читать дальшеИнтервал:
Закладка:









