Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Широкое применение в машиностроительной промышленности, а также в электротехнике и других производствах имеют различные сплавы меди с другими металлами. Важнейшими из них являются латуни (сплавы меди с цинком), медноникелевые сплавы и бронзы.
- 554 -
Латуни содержат до 45% цинка. Различают простые и специальные латуни. В состав последних, кроме меди и цинка, входят другие элементы, например железо, алюминий, олово, кремний. Латуни находят разнообразное применение. Из них изготовляют трубы для конденсаторов и радиаторов, детали механизмов, в частности часовых. Некоторые специальные латуни обладают высокой коррозионной стойкостью в морской воде и применяются в судостроении. Латунь с высоким содержанием меди — томпак — благодаря своему внешнему сходству с золотом используется для ювелирных и декоративных изделий.
Медноникелевые сплавы подразделяются на конструкционные и электротехнические. К конструкционным относятся мельхиоры и нейзильберы. Мельхиоры содержат 20-30% никеля и небольшие количества железа и марганца, а нейзильберы 5-35% никеля и 13-45% цинка. Благодаря стойкости против коррозии в воде, в том числе в морской, конструкционные медноникелевые сплавы получили широкое распространение в судостроении и в энергетической промышленности. Из них изготовляют радиаторы, трубопроводы, дистилляционные установки для получения питьевой воды из морской. К электротехническим медноникелевым сплавам относятся константан (40% Ni, 1.5% Mn) и манганин (3% Ni, 12% Mn), обладающие низким температурным коэффициентом электросопротивления и служащие для изготовления магазинов сопротивления, а также копель (43% Ni, 0.5% Mn), применяемый для изготовления термопар.
Бронзы подразделяются по основному входящему в их состав компоненту (кроме меди) на оловянные, алюминиевые, кремнистые и др. Из них оловянные представляют собой самые древние сплавы. На протяжении столетий они занимали ведущее место во многих отраслях производства. Сейчас применение их в машиностроении сокращается. Более широко применяются алюминиевые бронзы (5-10% Al и добавки Fe, Mn, Ni). Бериллиевые бронзы очень прочны и применяются для изготовления пружин и других ответственных деталей.
Все медные сплавы обладают высокой стойкостью против атмосферной коррозии.
В химическом отношении медь является малоактивным металлом. Однако с галогенами она реагирует уже при комнатной температуре, например, с влажным мором образует хлорид CuCl 2. О взаимодействии меди с кислородом воздуха говорилось выше, При нагревании медь взаимодействует и с серой, образуя сульфид Cu 2S.
Находясь в ряду напряжений после водорода, медь не вытесняет его из кислот. Поэтому соляная и разбавленная серная кислоты на медь не действуют.
- 555 -
Однако в присутствии кислорода воздуха медь растворяется в этих кислотах с образованием соответствующих солей:
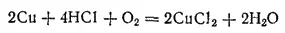
Летучие соединения меди окрашивают несветящее пламя газовой горелки в сине-зеленый цвет.
Известны соединения, в которых медь имеет степень окисленности один, два и три. Их можно рассматривать как производные соответствующих оксидов: Cu 2O, CuO и Cu 2O 3.
Соединения меди(I), в общем, менее устойчивы, чем соединения меди(II). Оксид Cu 2O 3и его производные весьма нестойки.
Оксид меди(I), или закись меди, Cu 2O встречается в природе в виде минерала куприта. Искусственно она может быть получена путем нагревания раствора соли меди(II) со щелочью и каким-нибудь сильным восстановителем, например формалином или глюкозой. При нагревании образуется осадок красного оксида меди(I).
В паре с металлической медью Cu 2O применяется в купроксных выпрямителях переменного тока.
При действии на Cu 2O соляной кислоты получается бесцветный раствор хлорида меди(I) CuCl. Если разбавить этот раствор водой, то хлорид меди(I) выпадает в виде белого творожистого осадка, нерастворимого в воде. Он может быть получен также кипячением раствора хлорида меди (II) CuCl 2с металлической медью в солянокислой среде:

Оксид меди(II), или окись меди, CuO — черное вещество, встречающееся в природе (например, в виде минерала тенорита). Его можно легко получить прокаливанием карбоната гидроксомеди(II) (CuOH) 2CO 3или нитрата меди(II) Cu(NO 3) 2. Оксид меди(II) проявляет окислительные свойства. При нагревании с различными органическими веществами CuO окисляет их, превращая углерод в диоксид углерода, а водород — в воду и восстанавливаясь при этом в металлическую медь. Этой реакцией пользуются при элементарном анализе органических веществ для определения содержания в них углерода и водорода.
Гидроксид меди(II) Cu(OH) 2осаждается из растворов солей меди(II) в виде голубой студенистой массы при действии щелочей. Уже при слабом нагревании даже под водой он разлагается, превращаясь в черный оксид меди(II).
Гидроксид меди(II) Cu(OH) 2- очень слабое основание. Поэтому растворы солей меди(II) в большинстве случаев имеют кислую реакцию, а со слабыми кислотами медь образует основные соли.
Важнейшими из солей меди(II) являются следующие.
Сульфат меди(II) CuSO 4в безводном состоянии представляет собой белый порошок, который при поглощении воды синеет. Поэтому он применяется для обнаружения следов влаги в органических жидкостях. Водный раствор сульфата меди имеет характерный сине-голубой цвет.
- 556 -
Эта окраска свойственна гидратированным ионам [Cu(H 2O) 4] 2+, поэтому такую же окраску имеют все разбавленные растворы солей меди(II), если только они не содержат каких-либо окрашенных анионов. Из водных растворов сульфат меди кристаллизуется с пятью молекулами воды, образуя прозрачные синие кристаллы. В таком виде он называется медным купоросом (см. стр. 376).
Хлорид меди(II) CuCl 2·2H 2O. Образует темно-зеленые кристаллы, легко растворимые в воде. Очень концентрированные растворы хлорида меди(II) имеют зеленый цвет, разбавленные — сине-голубой.
Нитрат меди(II) Cu(NO 3) 2·3H 2O. Получается при растворении меди в азотной кислоте. При нагревании синие кристаллы нитрата меди сначала теряют воду, а затем легко разлагаются с выделением кислорода и бурого диоксида азота, переходя в оксид меди(II).
Карбонат гидроксомеди(II) (CuOH) 2CO 3. Встречается в природе в виде минерала малахита, имеющего красивый изумруднозеленый цвет. Искусственно приготовляется действием Na 2CO 3на растворы солей меди(II):
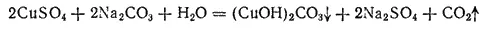
Интервал:
Закладка:








