Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:

При охлаждении раствора борная кислота выкристаллизовывается, так как в холодной воде она малорастворима.
При кипячении раствора борной кислоты вместе с парами воды отчасти улетучивается и борная кислота. Этим объясняется ее содержание в водяных парах, выделяющихся из трещин земли в вулканических местностях.
Борная кислота принадлежит к числу очень слабых кислот (при 20°C K 1=6·10 -10; K 2=2·10 -18; K 3=2·10 -14; ).
При нагревании борная кислота теряет воду, переходя сначала в метаборную кислоту HBO 2, а затем в борный ангидрид B 2O 3. Применяется борная кислота при приготовлении эмалей и глазурей, в производстве специальных сортов стекла, в бумажном и кожевенном производстве и в качестве дезинфицирующего средства.
Соли борных кислот — бораты — большей частью являются производными не ортоборной кислоты H 3BO 3, а четырехборной H 2B 4O 7и других более бедных водой борных кислот.
- 613 -
Тетраборат натрия, или бура, образует большие бесцветные прозрачные кристаллы состава Na 2B 4O 7·10H 2O, которые в сухом воздухе легко выветриваются. Бура получается при взаимодействии борной кислоты с гидроксидом натрия:
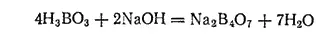
Водные растворы буры вследствие гидролиза обладают сильнощелочной реакцией.
При нагревании бура теряет кристаллизационную воду и плавится. В расплавленном состоянии она растворяет оксиды различных металлов с образованием двойных солей метаборной кислоты, из которых многие окрашены в цвета, характерные для каждого металла. На этом свойстве буры основано ее применение при сварке, резании и паянии металлов. Бура широко применяется в производстве легкоплавкой глазури для фаянсовых и фарфоровых изделий и особенно для чугунной посуды (эмаль). Кроме того, она используется при изготовлении специальных сортов стекла и в качестве удобрения, поскольку бор в малых количествах необходим растениям.
218. Алюминий (Aluminium).
Алюминий — самый распространенный в земной коре металл. Он входит в состав глин, полевых шпатов, слюд и многих других минералов. Общее содержание алюминия в земной коре составляет 8% (масс.).
Основным сырьем для производства алюминия служат бокситы, содержащие 32-60% глинозема Al 2O 3. К важнейшим алюминиевым рудам относятся также алунит K 2SO 4·Al 2(SO 4) 3·2Al 2O 3·6H 2O и нефелин Na 2O·Al 2O 3·2SiO 2.
СССР располагает запасами алюминиевых руд. Кроме бокситов, месторождения которых имеются у нас на Урале, в Башкирской АССР и в Казахстане, богатейшим источником алюминия является нефелин, залегающий совместно с апатитом в Хибинах. Значительные залежи алюминиевого сырья имеются в Сибири.
Впервые алюминий был получен Велером в 1827 г. действием металлического калия на хлорид алюминия. Однако, несмотря на широкую распространенность в природе, алюминий до конца XIX века принадлежал к числу редких металлов.
В настоящее время алюминий в громадных количествах получают из оксида алюминия Al 2O 3электролитическим методом. Используемый для этого оксид алюминия должен быть достаточно чистым, поскольку из выплавленного алюминия примеси удаляются с большим трудом. Очищенный Al 2O 3получают переработкой природного боксита.
Получение алюминия — сложный процесс, сопряженный с большими трудностями. Основное исходное вещество — оксид алюминия — не проводит электрический ток и имеет очень высокую температуру плавления (около 2050°C). Поэтому электролизу подвергают расплавленную смесь криолита Na 3[AlF 6] и оксида алюминия.
- 614 -
Смесь, содержащая около 10% (масс.) Al 2O 3, плавится при 960°C и обладает электрической проводимостью, плотностью и вязкостью, наиболее благоприятствующими проведению процесса. Для дополнительного улучшения этих характеристик в состав смеси вводят добавки AlF 3, CaF 2и MgF 2. Благодаря этому проведение электролиза оказывается возможным при 950°C.
Электролизер для выплавки алюминия представляет собой железный кожух, выложенный изнутри огнеупорным кирпичом. Его дно (под), собранное из блоков спрессованного угля, служит катодом. Аноды (один или несколько) располагаются сверху: это — алюминиевые каркасы, заполненные угольными брикетами. На современных заводах электролизеры устанавливают сериями; каждая серия состоит из 150 и большего числа электролизеров.
При электролизе на катоде выделяется алюминий, а на аноде — кислород. Алюминий, обладающий большей плотностью, чем исходный расплав, собирается на дне электролизера; отсюда его периодически выпускают. По мере выделения металла, в расплав добавляют новые порции оксида алюминия. Выделяющийся при электролизе кислород взаимодействует с углеродом анода, который выгорает, образуя СО и CO 2.
В дореволюционной России алюминий не производился. Первый в СССР алюминиевый завод (Волховский) вступил в строй в 1932 г., а уже в 1935 г. наша страна заняла по производству алюминия третье место в мире.
Одинаковое строение внешнего электронного слоя атома бора и алюминия обусловливает сходство в свойствах этих элементов. Так, для алюминия, как и для бора, характерна только степень окисленности +3. Однако при переходе от бора к алюминию сильно возрастает радиус атома (от 0,091 до 0,143 нм) и, кроме того, появляется еще один промежуточный восьмиэлектрониый слой, экранирующий ядро. Все это приводит к ослаблению связи внешних электронов с ядром и к уменьшению энергии ионизации атома (см. табл. 35). Поэтому у алюминия металлические свойства выражены гораздо сильнее, чем у бора. Тем не менее, химические связи, образуемые алюминием с другими элементами, имеют в основном ковалентный характер.
Другая особенность алюминия (как и его аналогов — галлия, индия и таллия) по сравнению с бором заключается в существовании свободных d-подуровней во внешнем электронном слое его атома. Благодаря этому координационное число алюминия в его соединениях может равняться не только четырем, как у бора, но и шести.
- 615 -
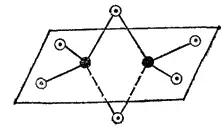
Рис. 165. Схема пространственного строения молекулы Al 2Cl 6: черные кружки — атомы алюминия, светлые — атомы хлора.
Соединенна алюминия типа AlЭ 3, как и аналогичные соединения бора, электронодефицитпьг в отдельных молекулах подобных соединений во внешнем электронном слое атома алюминия находится только шесть электронов. Поэтому здесь атом алюминия способен быть акцептором электронных пар. В частности, для галогенидов алюминия характерно образование димеров, осуществляемое по донорно-акцепторному способу (на схеме Г — атом галогена):
Читать дальшеИнтервал:
Закладка:








