Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
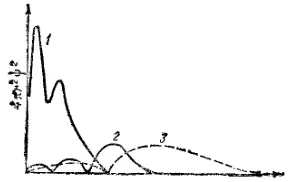
Рис. 21. График радиального распределения вероятности в атоме натрия.
1 — для десяти электронов K и L-слоев; 2 — для 3s-электрона; 3 — для 3p-электрона.
Так, в атоме натрия (порядковый номер Z = 11)ближайшие к ядру K- или L-слои заняты десятью электронами; одиннадцатый электрон принадлежит к M-слою (n=3). На рис. 21 кривая 1 изображает радиальное распределение вероятности для суммарного электронного облака десяти «внутренних» электронов атома натрия: ближайший к ядру максимум электронной плотности соответствует K-слою, второй максимум — L-слою. Преобладающая часть внешнего электронного облака атома натрия расположена вне области, занятой внутренними электронами, и потому сильно экранируется.
- 83 -
Однако часть этого электронного облака проникает в пространство, занятое внутренними электронами, и потому экранируется слабее.
Какое же из возможных состояний внешнего электрона атома натрия — 3s, 3p или 3d — отвечает более слабому экранированию и, следовательно, более сильному притяжению к ядру и более низкой энергии электрона? Как показывает рис. 21, электронное облако 3s-электрона в большей степени проникает в область, занятую электронами K- и L-слоев, и потому экранирует слабее, чем электронное облако 3p-электрона. Следовательно, электрон в состоянии 3sбудет сильнее притягиваться к ядру и обладать меньшей энергией, чем электрон в состоянии 3P. Электронное облако 3d-орбитали практически полностью находится вне области, занятой внутренними электронами, экранируется в наибольшей степени и наиболее слабо притягивается к ядру. Именно поэтому устойчивое состояние атома натрия соответствует размещению внешнего электрона на орбитали 3s.
Таким образом, в многоэлектронных атомах энергия электрона зависит не только от главного, но и от орбитального квантового числа. Главное квантовое число определяет здесь лишь некоторую энергетическую зону, в пределах которой точное значение энергии электрона определяется величиной l. В результате возрастание энергии по энергетическим подуровням происходит примерно в следующем порядке (см. также рис. 22 на стр. 90):
1s<2s<2p <3s<3p 4s<3d<4p<5s<4d<5p<6s<4f ≈ 5d < 6p<7s<5f ≈ 6d < 7p
32. Принцип Паули. Электронная структура атомов и периодическая система элементов.
Для определения состояния электрона в много электронном атоме важное значение имеет сформулированное В. Паули положение ( принцип Паули), согласно которому в атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковыми . Из этого следует, что каждая атомная орбиталь, характеризующаяся определенными значениями n, l и m, может быть занята не более чем двумя электронами, спины которых имеют противоположные знаки. Два таких электрона, находящиеся на одной орбитали и обладающие противоположно направленными спинами, называются спаренными, в отличие от одиночного ( т.е. неспаренного) электрона, занимающего какую-либо орбиталь.
Пользуясь принципом Паули, подсчитаем, какое максимальное число электронов может находиться на различных энергетических уровнях и подуровнях в атоме.
При l=0, т.е. на s-подуровне, магнитное квантовое число тоже равно нулю. Следовательно, на s-подуровне имеется всего одна орбиталь, которую принято условно обозначать в виде клетки («квантовая ячейка»): □.
- 84 -
Как указывалось выше, на каждой атомной орбитали размещается не более двух электронов, спины которых противоположно направлены. Это можно символически представить следующей схемой: 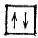
Итак, максимальное число электронов на s-подуровне каждого электронного слоя равно 2. При l=1 (p-подуровень) возможны уже три различных значения магнитного квантового числа (-1, 0, +1). Следовательно. На p-подуровне имеется три орбитали, каждая из которых может быть занята не более чем двумя электронами. Всего на p-подуровне может разместиться 6 электронов:
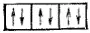
Подуровень d (l=2) состоит из пяти орбиталей, соответствующих пяти разным значениям m; здесь максимальное число электронов равно 10:
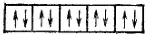
Наконец, на f-подуровне (l=3) может размещаться 14 электронов; вообще, максимальное число электронов на подуровне с орбитальным квантовым числом l равно 2(2l+1).
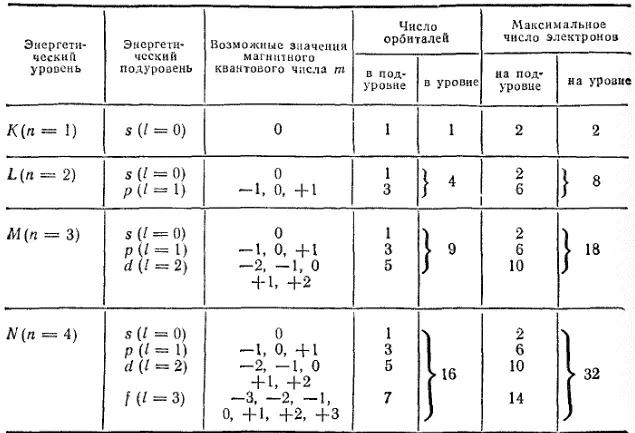
Первый энергетический уровень (K-слой, n=1) содержит только s-подуровень, второй энергетический уровень (L-слой, n=2) состоит из s- и p-подуровней и т.д. Учитывая этой, составим таблицу максимального числа электронов, размещающихся в различных электронных слоях (табл. 2).
Как показывают приведенные в табл. 2 данные, максимальное число электронов на каждом энергетическом уровне равно 2n 2, где n — соответствующее значение главного квантового числа. Так, в K-слое может находиться максимум 2 электрона (2·1 2=2), в L-слое — 8 электронов (2· 2 2=8), в M-слое — 18 электронов (2· 3 2=18) и т.д. Отметим, что полученные числа совпадают с числами элементов в периодах периодической системы.
Наиболее устойчивое состояние электрона в атоме соответствует минимальному возможному значению его энергии . Любое другое его состояние является возбужденным, неустойчивым: из него электрон самопроизвольно переходит в состояние с более низкой энергией. Поэтому в невозбужденном атоме водорода (заряд ядра Z = 1) единственный электрон находится в самом низком из возможных энергетических состояний, т.е. на 1s-подуровне. Электронную структуру атома водорода можно представить схемой
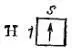
или записать так: 1s 1(читается «один эс один»).
- 85 -
Таблица 2. Максимальное число электронов на атомных энергетических уровнях и подуровнях
В атоме гелия (Z =2) второй электрон также находится в состоянии 1s. Его электронная структура (1s 2— читается «один эс два») изображается схемой:
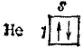
У этого элемента заканчивается заполнение ближайшего к ядру K-слоя и тем самым завершается построение первого периода системы электронов.
У следующего за гелием элемента — лития (Z=3) третий электрон уже не может разместиться на орбитали K-слоя: это противоречило бы принципу Паули. Поэтому он занимает s-состояние второго энергетического уровня (L-слой, n=2). Его электронная структура записывается формулой 1s 22s 1, что соответствует схеме:
Читать дальшеИнтервал:
Закладка:






