Михаил Супотницкий - Эволюционная патология
- Название:Эволюционная патология
- Автор:
- Жанр:
- Издательство:Вузовская книга
- Год:2009
- Город:Москва
- ISBN:978-5-9502-0378-7
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Михаил Супотницкий - Эволюционная патология краткое содержание
Книга рассчитана на широкий круг читателей. Особенно полезной она будет для исследователей, интересующихся фундаментальными проблемами патогенеза и эпидемиологии новых инфекционных болезней, для студентов биологических и медицинских факультетов вузов, а также для врачей-инфекционистов и эпидемиологов.
Книга издана в авторской редакции.
Эволюционная патология - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Выделены два класса автономных ретроэлементов: не-LTR (non-LTR) и LTR-элементы (LTR-elements), структурно сходные с ретровирусами, но утратившие функционирующий env ген.
Длинные концевые повторы или LTR (long terminal repeats) — это прямые повторяющиеся последовательности на концах ДНК-копии генома ретровирусов, образовавшейся в результате обратной транскрипции. Каждый такой повтор состоит из трех элементов: U3-R-U5, длина которых составляет соответственно 170–1250, 10–80 и 80–100 т. п. н.; 3’-конец U5 сам содержит короткий инвертированный повтор, гомологичный последовательности на 5'-конце элемента U3, т. е. сама последовательность LTR фланкирована короткими инвертированными повторами; LTR участвуют в интеграции ДНК-копии генома ретровируса в геном клетки-хозяина, кроме того, область U3 каждого LTR несет промотор, причем промотор левого LTR участвует в транскрипции ДНК провируса, а промотор правого — последовательности ДНК клетки-хозяина вблизи сайта интеграции ретровируса. LTR фланкируют сложные элементы генома и участвуют в процессе их транспозиции (Khodosevich K. et al., 2002).
Неавтономные ретротранспозоны не кодируют белков. К ним относятся Alu — повторы (в геноме человека их более миллиона; см. «Эволюционная роль Alu-элементов»); псевдогены, образовавшиеся в результате обратной транскрипции (см. «Эволюционная роль псевдогенов»); и SVA — элементы (аббревиатура от заглавных букв SINE — R, VNTR и Alu , описаны как «композитные ретропозоны; более подробно о SVA — элементах см. в подглаве 4.3). Для своей транспозиции они нуждаются в активности автономных ретроэлементов. Например, SVA-элементы ретротранспозируются с помощью L1-транспозонов (более подробно о транспозиции неавтономных ретротранспозонов см. в работе Ostertag E. M., Kazazian H., 2001).
Не-LTR-ретроэлементы. Очень древние ретроэлементы. Широко представлены среди простейших организмов. Два представителя этого семейства ретроэлементов встречаются в геноме человека в очень больших количествах. Это короткие вставочные элементы (short interspersed elements, SINE) с преобладанием Alu- и MIR-повторов; и длинные терминальные вставочные повторы (long-terminal interspersed elements, LINE), представленные автономными L1 и L2 последовательностями (см. «Эволюционная роль L1 ретроэлементов»). SINE обычно имеют длину 100–400 п. о. и по большей части происходят от транскриптов генов тРНК, синтезированных посредством РНК-полимеразы III (pol III). SINE имеют внутренний промотор, который позволяет их транскрипцию РНК-полимеразой III. Они не имеют емкости, достаточной для поддержания генов амплификации, и их размножение в геноме человека зависит от LINE.
LTR-ретроэлементы. Составляют до 8 % генома человека. К ним относятся ретротранспозоны (retrotransposons), эндогенные ретровирусы (endogenous retroviruses, ERVs), человеческие эндогенные ретровирусы (human endogenous retroviruses, HERVs) и повторяющиеся элементы эндогенных ретровирусов человека (repeat elements with HERV origin), такие как SINE-R ретропозоны (SINE-R retroposons). Последние содержат участки последовательностей LTR HERV-K (рис. 3).
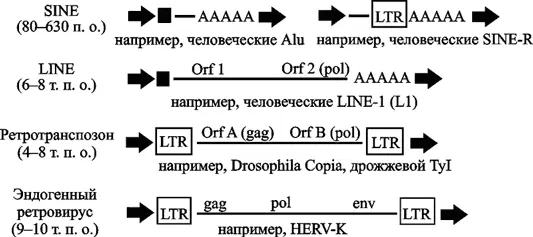
Стрелками показаны повторяющиеся последовательности, образованные во время интеграционных процессов. Заполненные квадраты соответствуют промоторным регионам. А-последовательности показывают первоначальное полиаденилирование (original polyadenylation). Сокращения: bp — пары оснований; Orf — открытая рамка считывания; LTR — длинные концевые повторы (по Bannert N., Kurth R., 2004).
В геноме человека содержится не менее 98 тыс. ERV (Paces J. et al., 2002). Ген env ERV придает способность ретровирусу распространяться между клетками и индивидуумами. Отдельные LTR эндогенных ретровирусов и ретротранспозоны, образовавшиеся благодаря рекомбинационным процессам, в которых участвуют сами LTR-ретроэлементы, встречаются в геноме человека на один-два порядка чаще, чем эндогенные ретровирусы. Всего выделяется 6 суперсемейств LTR-ретроэлементов (табл. 2).
[4] По P. Medstrand, L. N. van de Lagemaat, D. L. Mager (2002).
Элемент | Характеристика
Класс I ERV | Сходен с типом С или гамма-ретровирусами
Класс II ERV | Сходен с типом B или бета-ретровирусами
Класс III ERV | Отдаленно связан со спума-ретровирусами
MER4 | Неавтономный, связанный с ERV
MST | Названы по общему MstII рестрикционному сайту
MLT | LTR транспозоны млекопитающих
Принимая во внимание то, что эндогенные ретровирусы классов I и II проникли в зародышевую линию примитивных приматов как инфекционные ретровирусы и в последующем подвергались взрывной амплификации и транспозиции в периоды активной эволюции приматов, другие суперсемейства, вероятно, соответствуют древним ретротранспозонам, которые амплифицировались на ранних этапах эволюции млекопитающих. Только небольшая часть «молодых» субтипов Alu и L1 non-LTR-элементов остаются активными в геноме человека (Medstrand P. et al., 2002).
В механизме «перехода» экзогенного ретровируса в эндогенный много неясного. Эндогенизации у людей известных экзогенных ретровирусов пока не зафиксировано. Вероятность таких событий для генома нашего вида нельзя исключать, так как сходные процессы обнаружены у других млекопитающих. Например, вирус рака молочной железы мышей (mouse mammary tumor virus, MMTV), вирус мышиной лейкемии (murine leukemia viruses), вирус птичьей лейкемии (avian leukemia viruses, ALV) и вирус кошачьей лейкемии (feline leukemia virus, FeLV) встречаются у своих хозяев как в эндо-, так и в экзовариантах (Medstrand P., Mager D. L.,1998). Как будет показано ниже (см. «Эволюционная роль HERV-K»), эндогенизация ретровирусов у гоминид происходит не только очень редко (в масштабах времени скорее геологических, чем отражающих продолжительность существования вида), но и в периоды каких-то важных эволюционных событий для этого семейства в целом.
Попытки таксономии эндогенных ретровирусов человека приводят ученых к замешательству. Предпочтительным приемом таких исследований является использование аминокислотной специфичности тРНК, которая гибридизуется с праймер-связывающим сайтом (primer-binding site). Например, HERV-K использует лизинспецифическую тРНК как праймер для инициации реакции обратной транскрипции. Но сегодня известно, что весьма различные ретровирусы используют этот же праймер. Кроме того, неполная информация по коротким участкам вирусов, содержащим мутации и делеции, делает их классификацию почти невозможной. К этому надо добавить лабораторные ошибки, когда отдельные ретровирусы выделяются и именуются произвольно в разных лабораториях (Bannert N., Kurth R., 2004).
Эволюционная роль HERV-K.Наиболее вероятной схемой появления в геноме человека мультикопийных семейств HERV, N. de Parseval и T. Heidmann (2005) считают следующую: экзогенные ретровирусы случайно инфицируют клетки зародышевой линии (germline cells) во время развития плода. После первичной «колонизации» генома ставшие эндогенными ретровирусы передаются вертикально. Амплификация копий «предкового» провируса осуществляется путем внутриклеточной ретротранспозиции и повторной интеграции в клетки зародышевой линии. Каждая новая колонизация таких клеток дает новое семейство или линию ERV.
Читать дальшеИнтервал:
Закладка:








![Михаил Супотницкий - Очерки истории чумы. Книга II. Чума бактериологического периода [без иллюстраций]](/books/1084186/mihail-supotnickij-ocherki-istorii-chumy-kniga-ii.webp)
![Михаил Супотницкий - Очерки истории чумы. Книга I. Чума добактериологического периода [без иллюстраций]](/books/1084187/mihail-supotnickij-ocherki-istorii-chumy-kniga-i-ch.webp)
