Борис Степин - Книга по химии для домашнего чтения
- Название:Книга по химии для домашнего чтения
- Автор:
- Жанр:
- Издательство:Химия
- Год:1994
- Город:М.
- ISBN:5-7245-0708-0
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Борис Степин - Книга по химии для домашнего чтения краткое содержание
В виде небольших рассказов, заметок и ответов на вопросы приведены сведения из различных разделов химии и эпизоды из жизни ученых-химиков. Цель книги — дать читателю представление о химии как о необходимом звене, гармонично связывающем нас с природой, позволяющем создавать необходимые цивилизованному миру предметы и материалы.
Книга рассчитана на широкий круг читателей — преподавателей и студентов, школьников и пенсионеров, инженеров и домохозяек. Любознакльные найдут здесь интересные факты, а практичные читатели — полезные советы и рекомендации.
Книга по химии для домашнего чтения - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
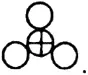
Воду он изображал символом

Алхимические обозначения не включали символов химических элементов, не характеризовали состав вещества, а представляли лишь условное его изображение, с помощью которого алхимики зашифровывали свои «секреты», причем почти у каждого из них был свой набор подобных знаков, известный только ему одному.
Первый значительный шаг в изображении химического состава веществ сделали во Франции инженер Жак-Анри Гассенфратц (1755–1827) и химик и врач Пьер-Огюст Аде (1763–1834). Они вместо алхимических символов веществ и семи металлов ввели обозначение известных химических элементов в виде дуг, черточек и кружочков, в которые помещали первую букву французского названия элемента. Из таких символов начали составлять химические формулы веществ. Затем Дальтон (см. 2.8) ввел в употг ребление свои символы химических элементов и также использовал их для обозначения состава веществ (табл. 2).
3.3. «СПИРИТУС НИТРИ» РАСТВОРЯЕТ «ВЕНЕРУ», «МАРС» И «ЛУНУ». ЧТО ЭТО ЗНАЧИТ?
Аптекари XVI в. в России концентрированную азотную кислоту HNO 3называли «спиритус нитри» (см. 1.48; 5.50). «Венера», «марс» и «луна» — это названия металлов (см. табл. 1) — меди Cu, железа Fe и серебра Ag.
Азотная кислота взаимодействует с этими металлами так:
В первой реакции образуется нитрат серебра AgNO 3, во второй — нитрат меди Cu(NO 3) 2, в третьей — нитрат железа Fe(NO 3) 3. Во всех приведенных реакциях выделяется бурого цвета газ — диоксид азота NO 2.
3.4. ХИМИЧЕСКИЕ ЗАПИСИ ПЕТРА I
В бумагах Петра I, датированных 1720 г., были обнаружены записи химических реакций и символов:
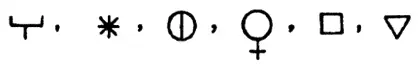
Петр I использовал алхимическую символику (см. 3.2) для обозначения следующих веществ соответственно слева направо: карбоната калия K 2CO 3, или поташа; хлорида аммония NH 4Cl, или нашатыря; нитрата калия KNO 3, или селитры; меди Си, мочи, воды H 2O.
3.5. СИСТЕМА СИМВОЛОВ БЕРЦЕЛИУСА
Торнберн-Улаф Бергман (1735–1784) — шведский химик и минералог, член Шведской королевской академии наук — советовал в последние годы своей жизни французскому химику Гитону де Морво, инициатору создания первой номенклатуры химических веществ: «Не щадите ни одного неправильного наименования, знающие поймут всегда, незнающие поймут тем скорее».
Шведский химик Берцелиус (см. 2.19) использовал этот совет для разработки своей системы химических символов, которая сохранилась и в современной химии. Он предложил в качестве символов химических элементов принимать первую букву их латинских названий, а в случае совпадения первых букв — использовать и вторую букву. Так, для обозначения кислорода он взял символ «О» — первую букву от Oxygenium (оксигениум), для водорода — «Н» — от Hydrogenium (гидрогениум), для углерода — «С» — от Carboneum (карбонеум). Символ химического элемента кальция «Ca» уже содержит две первые буквы слова Calcium (кальциум) — во избежание совпадения с символом углерода. Две буквы нужны и для символа химического элемента меди: «Cu» от Cuprum (купрум) — по той же причине.
Если же кислород входит в состав сложного вещества, то Берцелиус рекомендовал пользоваться точками над символом элемента.
Например, Ċa — оксид кальция CaO;
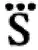
— серная кислота H 2SO 4;

— азотная кислота с формулой HNO 3. Если в составе вещества два атома одинакового вида, Берцелиус предлагал ставить поперечную черту на расстоянии 1/ 3от нижней части символа:
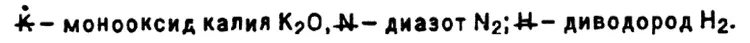
Реакция получения аммиака NH 3взаимодействием хлорида аммония NH 4Cl и оксида кальция CaO по Берцелиусу записывалась так:
Современная запись этой реакции:
Уже после Берцелиуса число атомов в соединениях стали указывать цифрами справа вверху символа химического элемента. Например, K 2SO 4— сульфат калия, NH 3— аммиак, Al 2O 3— оксид алюминия. Надстрочные индексы в формулах соединений сохранились до конца XIX в. и использовались Менделеевым во всех восьми изданиях его знаменитого учебника «Основы химии». Принятое в настоящее время указание числа атомов в молекулах соединений подстрочной цифрой (K 2SO 4, NH 3) было предложено еще в 1834 г. Либихом (см. 2.17).
3.6. СОЛИ ТАХЕНИЯ
Содержание понятия «соль» впервые раскрыл немецкий аптекарь Отто Тахений (1620–1699). В одном из своих сочинений он писал: «Все соли состоят из какой-либо кислоты и из какой-либо щелочи… из этих двух универсальных принципов составлены все тела мира».
Сейчас мы с вами знаем, что соли — продукты реакций замещения атомов водорода кислоты на металл или гидроксид-ионов OH-оснований на анионы кислот. При полном замещении атомов водорода образуются средние соли, например K 2SO 4— сульфат калия, а при неполном — кислые, например KHSO 4— гидросульфат калия. При взаимодействии некоторых солей с водой (реакции гидролиза) образуются основные соли. В частности, в реакции сульфата меди CuSO 4с водой в растворе появляется основный сульфат меди (CuOH) 2SO 4:
Соли являются, как правило, кристаллическими веществами, состоящими из катионов и анионов.
3.7. ХИМИЯ БЕЗ ФОРМУЛ
Почему в работах таких выдающихся химиков XVIII–XIX вв., как Либих, Дэви, Фарадей, Бертло и др., нельзя найти ни одной химической формулы?
У химиков того времени еще не было общепринятого «химического языка» — формул. Вещества и реакции описывались только словами. Например: «Я растворил в пол-унции горячей азотной кислоты драхму серебра и налил туда две унции спирта», — так описывает Либих свой способ приготовления «гремучего серебра» (см. 3.26).
Теперь реакцию Либиха по получению фульмината серебра («гремучего серебра» AgCNO) записывают в виде уравнения
Иногда химики пользовались символами собственного изобретения, которых не понимал никто, кроме их авторов. Например, в статье 1820 г. можно встретить такую формулу:
C трудом удалось установить, что L — известь Ca(OH 2), S — кремнезем SiO 2, О — кислород, W — вода. Что означало все это вместе, сказать трудно.
Даже к концу XIX в. формулу, например, этанола C 2H 5OH изображали по-разному: Либих (C 4H 15)O, H 2O; Дюма — C 4H 8+ H 4O 2; Берцелиус — (C 2H 6)O.
Читать дальшеИнтервал:
Закладка:










