Борис Степин - Книга по химии для домашнего чтения
- Название:Книга по химии для домашнего чтения
- Автор:
- Жанр:
- Издательство:Химия
- Год:1994
- Город:М.
- ISBN:5-7245-0708-0
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Борис Степин - Книга по химии для домашнего чтения краткое содержание
В виде небольших рассказов, заметок и ответов на вопросы приведены сведения из различных разделов химии и эпизоды из жизни ученых-химиков. Цель книги — дать читателю представление о химии как о необходимом звене, гармонично связывающем нас с природой, позволяющем создавать необходимые цивилизованному миру предметы и материалы.
Книга рассчитана на широкий круг читателей — преподавателей и студентов, школьников и пенсионеров, инженеров и домохозяек. Любознакльные найдут здесь интересные факты, а практичные читатели — полезные советы и рекомендации.
Книга по химии для домашнего чтения - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Добавим, что благодаря своим окислительным свойствам и наглядному изменению окраски в химических реакциях перманганат калия нашел широкое применение в химическом анализе.
5.48. ПРОДЕЛКИ ИМИТАТОРА
Некий фокусник пообещал изумленным зрителям продемонстрировать превращение фиолетовых кристаллов квасцов в изумруд, топаз, янтарь или сапфир.
Настоящие драгоценные камни получить из квасцов (см. 151; 3.21), конечно, не удастся. А вот растворы, имитирующие цвета изумруда (см. 10.22), топаза (см. 10.33), янтаря (см. 10.1), сапфира (см. 10.42), получить можно. Для этого фокуснику придется запастись химическими реактивами. Растворив хромокалиевые квасцы [кристаллогидрат сульфата хрома-калия KCr(SO 4) 2∙12Н 2O] в воде, он получит фиолетовый раствор; обработка этого раствора избытком гидроксида калия KOH или натрия NaOH приведет к образованию раствора изумрудного цвета:
Зеленый цвет обусловлен присутствием гексагидроксохромата калия К 3[Cr(ОН) 6]. Если к этому раствору добавить пероксид водорода H 2O 2, то зеленый цвет раствора сменяется на желтый, цвет топаза:
Такая окраска раствора обусловлена присутствием хромата калия K 2CrO 4. При подкислении желтого раствора серной кислотой H 2SO 4появляется оранжевая окраска, напоминающая цвет янтаря:
Водный раствор дихромата калия K 2Cr 2O 7имеет оранжевый цвет. Наконец, добавляя к такому раствору пероксид водорода и диэтиловый эфир (C 2H 5) 2O, можно получить сложное пероксосоединение CrO(O 2) 2∙(C 2H 5) 2O, окрашивающее слой эфира в ярко-синий, «сапфирный» цвет.
5.49. ЗАГАДКА ДИХЛОРИДА
Химик обнаружил в шкафу запечатанную банку без надписи с кристаллами зеленого цвета внутри. Сохранился лишь обрывок этикетки со словом «дихлорид». При контакте этих зеленых кристаллов с водой раствор оказался фиолетовым; потом из этой фиолетовой жидкости начали выделяться пузырьки газа, а спустя несколько секунд она стала зеленой. При смешивании раствора сульфата меди CuSO 4с теми же зелеными кристаллами выделились крупинки металлической меди… Какой дихлорид был в банке?
Не так уж много дихлоридов имеет зеленый цвет. Это, во-первых, тетрагидрат хлорида железа FeCl 2∙4Н 2O, гексагидрат хлорида никеля NiCl 2∙6Н 2O, безводные дихлориды меди CuCl 2, иридия IrCl 2и платины PtCl 2и безводный дихлорид ванадия VCl 2. Дихлориды иридия и платины в воде практически нерастворимы, дихлориды железа, меди и никеля дают зеленый (для железа — быстро желтеющий на воздухе) водный раствор, газы при этом не выделяются. Значит, дихлорид ванадия? Действительно, зеленые кристаллы VCl 2образуют фиолетовый раствор, из которого выделяется водород, а окраска раствора становится зеленой:
Очевидно, ванадий в степени окисления (+II) настолько сильный восстановитель, что выделяет водород даже из воды. Не удивительно, что он осаждает и медь Cu из раствора сульфата меди CuSO 4, превращаясь в хлорид оксопентаакваванадия(IV):
окрашивающего раствор в синий цвет.
5.50. ЧТО ТАКОЕ КРАСНАЯ АЗОТНАЯ КИСЛОТА?
Термин «дымящая красная азотная кислота» использовался вплоть до сороковых годов нашего века (см. 1.48). Это раствор диоксида азота NO 2в азотной кислоте HNO 3. Он может быть получен как насыщением концентрированной азотной кислоты диоксидом азота, так и путем взаимодействия компонентов смеси, содержащей 2 моль нитрата натрия NaNO 3и 1 моль серной кислоты H 2SO 4при нагревании. Сначала при 100-110ºC, согласно уравнению
из смеси выделяется и перегоняется чистая азотная кислота HNO 3. Если повысить температуру до 150–170°С, то в реакцию вступает образовавшийся в растворе гидросульфат натрия NaHSO 4:
и одновременно большая часть азотной кислоты начинает разлагаться с выделением диоксида азота и кислорода:
Диоксид азота, растворяясь в первых порциях отгоняемой азотной кислоты, и сообщает ей красно-оранжевый цвет. Никакого другого красителя здесь нет.
5.51. ДО ПОСИНЕНИЯ…
Каждая хозяйка и каждый школьник знают: крахмал, на который попал иод, синеет. Почему?
Крахмал состоит из длинных полимерных молекул, построенных из фрагментов глюкозы:
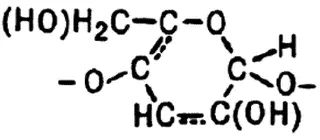
и закрученных по спирали так, что глюкозные шестиугольники образуют длинный цилиндрический канал. Молекулы иода I 2«забираются» в этот канал, превращаются в нем в линейные анионы [I 5]-, отрывающие от фрагментов глюкозы электроны и выстраивающиеся длинной цепочкой:
…[ I 2—I -—I 2] … [I 2— I -—I 2]…
Так образуется соединение включения, называемое иногда «канальным» соединением, оно-то и имеет синюю окраску.
5.52. ЧЕМ ПРИМЕЧАТЕЛЬНЫ «БУРГУНДСКАЯ» И «БОРДОСКАЯ ЖИДКОСТИ»?
Оба препарата применяются садоводами и огородниками для борьбы с возбудителями грибковых болезней плодовых, овощных и декоративных культур. Обе жидкости готовят добавлением к водному раствору сульфата меди CuSO 4∙5Н 2O (медного купороса, см. 1.47), либо порошка гидроксида кальция Ca(OH) 2(гашеной извести, см. 323), либо карбоната натрия Na 2CO 3(соды, см. 1.19–1.22):
В первой реакции образуется суспензия гидроксида меди Cu(OH) 2и сульфата кальция CaSO 4, называемая «бордоской жидкостью», во второй — суспензия основного карбоната меди (CuOH) 2CO3, получившая название «бургундской жидкости».
5.53. «ФИЛОСОФСКАЯ ШЕРСТЬ»
При горении парообразного цинка на воздухе появляется сине-зеленое пламя и образуются белые хлопья оксида цинка ZnO. В Средние века этот оксид называли «философской шерстью» из-за его волокнистого строения и способности участвовать во многих не всегда понятных реакциях.
Оксид цинка в виде белого порошка используется для приготовления цинковых белил. Однако, применяя эту краску, помните, что оксид цинка при нагревании желтеет, правда, при охлаждении желтизна медленно исчезает. Кстати, если в краску, наряду с оксидом цинка, добавить карбонат цинка ZnCO 3(тоже белое вещество), то краска приобретет свойство антипирена, огнезащитного вещества: при сильном нагреве начнется ее разложение с выделением диоксида углерода CO 2:
который препятствует распространению огня.
Читать дальшеИнтервал:
Закладка:










