Валерий Крылов - Каталитический риформинг бензинов. Теория и практика
- Название:Каталитический риформинг бензинов. Теория и практика
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:2021
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Валерий Крылов - Каталитический риформинг бензинов. Теория и практика краткое содержание
В книге представлен анализ теоретических и практических положений технологии процесса каталитического риформинга бензиновых фракций. Изложен опыт и приведены лучшие практики эксплуатации современных установок риформинга.
Книга предназначена для инженерно-технических работников нефтеперерабатывающих заводов, проектных организаций, преподавателей и студентов вузов.
Каталитический риформинг бензинов. Теория и практика - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Роль этой реакции определяется тем, что ароматизация парафинов на бифункциональных катализаторах проходит преимущественно по механизму С 5-дегидроциклизации с промежуточным образованием метилциклопентана и его гомологов, поэтому реакция изомеризации циклопентанов является необходимой стадией для образования бензола и его гомологов.
При температуре 800 К изменение энергии Гиббса для этой реакции положительно, и константа K pравняется 0,08. Это означает, что в равновесной смеси доля метилциклопентана составляет 92,6 % мол.
Поскольку в реальном сырье риформинга отношение
«циклогексан/метилциклопентан» значительно выше равновесного значения, то термодинамика запрещает протекание реакции в прямом направлении, а это делает принципиально невозможным ароматизацию парафиновых углеводородов, которая тем не менее в реальных условиях успешно осуществляется через механизм С 5-циклизации. Данное противоречие разрешается при включении в цепочку превращений реакции дегидрирования циклогексана в бензол, которая имеет большое негативное изменение энергии Гиббса. В этом случае суммарное превращение происходит со значительным уменьшением энергии Гиббса (рис. 7).
Действительно, итоговая реакция является суммой реакции изомеризации и дегидрирования.
Поскольку энергия Гиббса является функцией состояния и не зависит от пути перехода, то для итоговой реакции
Δ г G o = +16,8 + (–96,6) = –79,8.
Отсюда константа равновесия может быть определена как произведение констант равновесия реакций изомеризации и дегидрирования или как exp (–Δ г G o/RT) и составит
K p = 1,19·10 5.
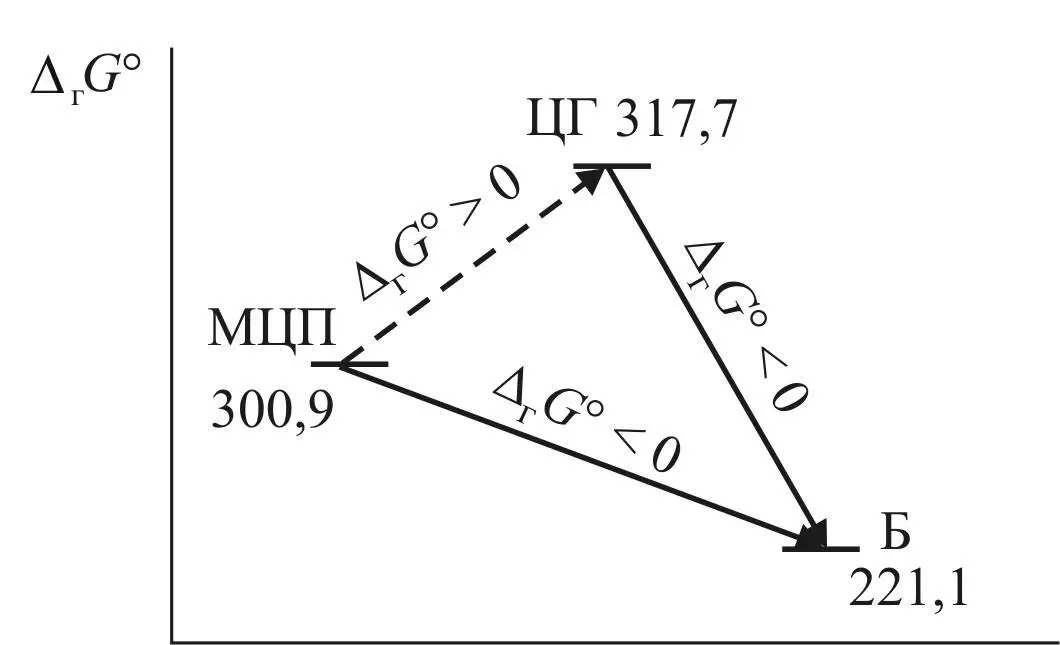
Рис. 7. Изменение энергия Гиббса
в реакции ароматизации метилциклопентана
Механическим аналогом сопряженных химических реакций является устройство, приведенное на рис. 8 [31].
Устройство представляет собой два груза, соединенных канатом.
Сам по себе подъем легкого груза невозможен, это не самопроизвольный процесс, но он становится возможным, если сопровождается опусканием тяжелого груза. Условием, необходимым для сопряжения двух процессов, является наличие механической связи между двумя грузами.
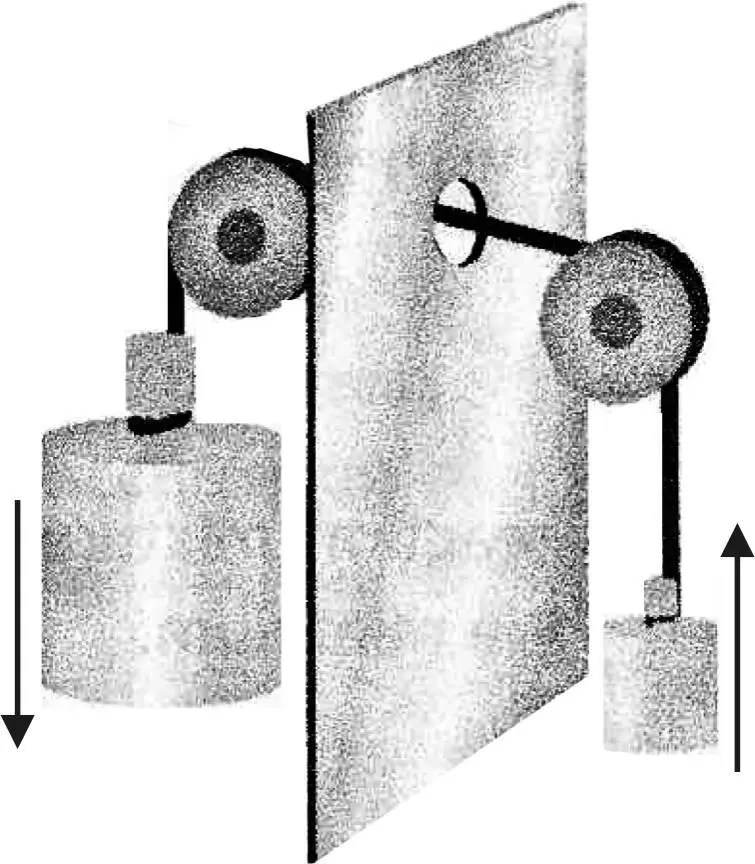
Рис. 8. Механический аналог сопряженных
химических реакций
В химической системе такое сопряжение достигается, если продукт одной химической реакции может расходоваться в другой.
Рассмотренный случай (см. рис. 6) является одним из многих примеров того, как одиночная реакция, невозможная с позиции термодинамики, становится возможной при сопряжении с другой реакцией, обеспечивающей снижение энергии Гиббса для суммарного превращения.
Влияние температуры и давления на константы химического равновесия. Связь изменения температуры и K рустанавливается уравнением Вант – Гоффа:
d ln K р/ dT = Δ H / R T 2,
где Δ H – тепловой эффект реакции. Характер зависимости определяется знаком и величиной теплового эффекта реакции.
В соответствии с уравнением Вант – Гоффа увеличение температуры приводит к увеличению K рэндотермических реакций (Δ H > 0) и возрастанию равновесной степени превращения.
Этот же результат вытекает из принципа Ле Шателье: внешнее воздействие на систему, находящуюся в равновесии, приводит к таким изменениям в системе, которые компенсируют эффект внешнего воздействия.
Наибольшее влияние изменение температуры оказывает на реакции дегидрирования нафтенов и дегидроциклизации парафинов, которые имеют самые высокие значения теплового эффекта. Так, при температуре 800 К изменение энергии Гиббса для суммарной реакции превращения метилциклопентана в бензол составляет, по данным табл. 2, 16,8 + (–96,6) = –79,8 кДж/моль. Этому значению соответствует K р1,52Е + 5.
При снижении температуры до 500 К изменение потенциала становится равным +26,1 кДж/моль, и константа равновесия снижается до 1,29; это означает, что в данных условиях суммарная реакция меняет направление и проходит с образованием метилциклопентана.
Ниже приведены расчетные значения энергии Гиббса для температуры в интервале 500–800 К:
Т , К
Δ г G , кДж/моль
800
–79,8
700
–44,2
600
–8,8
500
+26,1
Для наглядности ниже представлены графики изменений потенциалов для двух температур: 800 и 500 К (рис. 9).
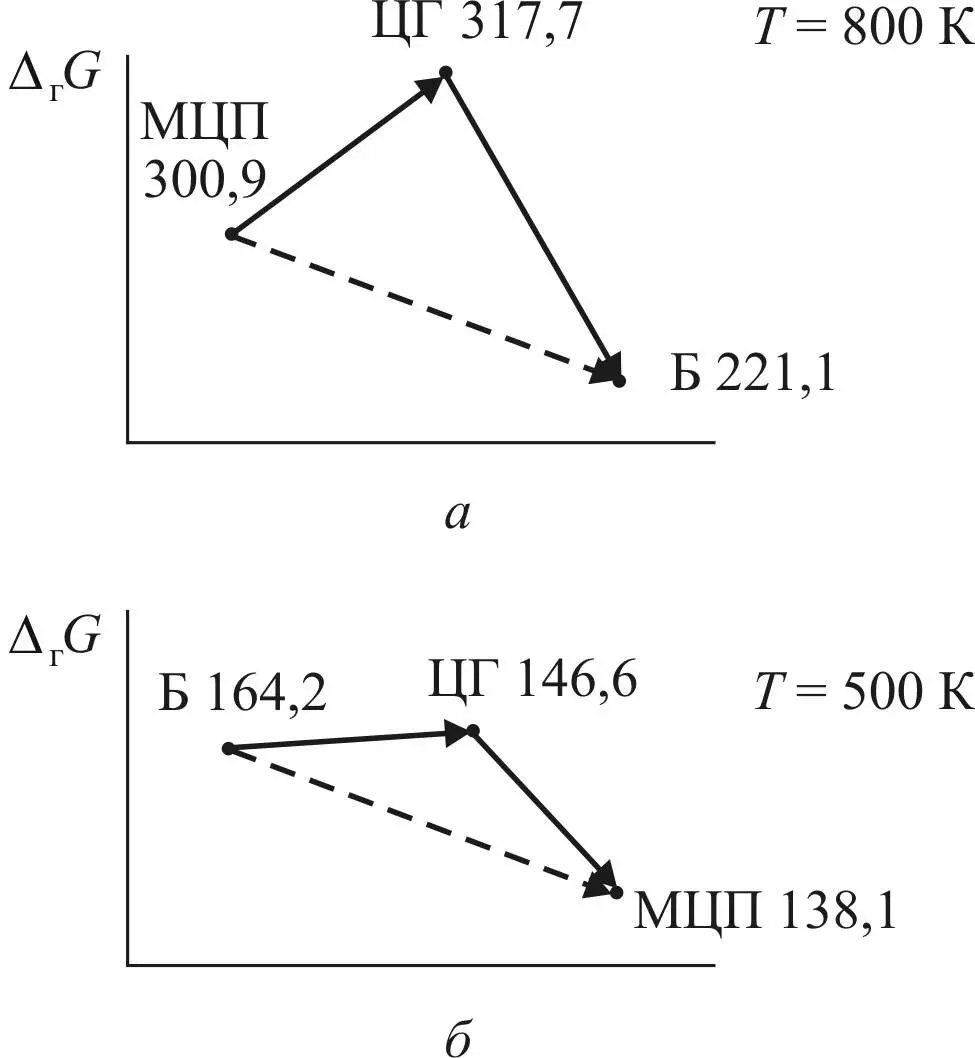
Рис. 9. Изменения потенциалов Гиббса
для двух температур: а – 800 К; б – 500 К
Константа равновесия реакции дегидрирования алканов при температурах платформинга имеет низкое значение, в связи с этим олефины в заметных количествах появляются в продуктах риформинга только при проведении процесса при очень низком давлении, реализуемом на установках платформинга с непрерывной регенерацией катализатора.
Вместе с тем, поскольку эндотермичность реакции обусловливает увеличение константы равновесия при повышении температуры, при достаточно высоких температурах олефины могут быть основным продуктом превращения. Примерами таких процессов являются процессы дегидрирования и термический риформинг.
В целом повышение температуры процесса благоприятствует протеканию основных реакций дегидрирования и дегидроциклизации, что приводит к более глубокой ароматизации сырья.
Давление и константы равновесия связаны уравнением
где K y– константа равновесия, выраженная в мольных долях реагирующих веществ; сумма ν – изменение стехиометрических коэффициентов реагирующих веществ.
Давление не влияет на величину константы равновесия K р, которая зависит только от температуры, но может изменять величину K y, связанную с составом равновесной смеси.
Давление не оказывает влияния на состав равновесной смеси для реакций изомеризации и крекинга, для которых сумма стехиометрических коэффициентов в химическом уравнении равна нулю, в этом случае K y = K р.
Наиболее чувствительны к изменению давления реакции дегидрирования нафтенов и дегидроциклизации парафинов. Рост давления оказывает негативное влияние на эти реакции и уменьшает термодинамически возможную степень ароматизации сырья платформинга.
Эффект изменения давления показан на примере расчета состава равновесной смеси для превращения циклогексана при давлении 30 и 10 атм (температура 800 К).
Схема реакций:
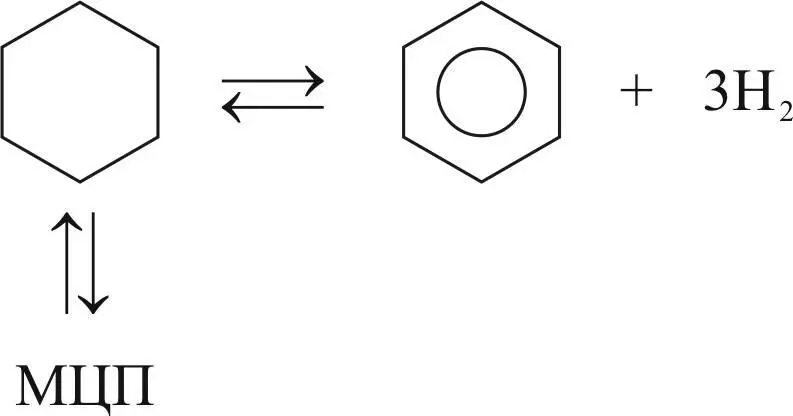
Для расчета мольных долей четырех компонентов равновесной смеси используется система уравнений
Читать дальшеИнтервал:
Закладка:









