Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Качественная реакция – помутнение раствора хлорида палладия(II).
Применяется как реагент в органическом синтезе, промышленно важный восстановитель металлов из их руд.
Чрезвычайно ядовит, загрязняет атмосферу городов (продукт неполного сгорания моторного топлива). По тому же механизму, что и кислород, СО присоединяется к атому железа в гемоглобине крови, причем связывается более прочно и тем самым блокирует перенос кислорода в организме, вызывая сильное отравление и остановку дыхания; отсюда тривиальное название СО — угарный газ.
Уравнения важнейших реакций:
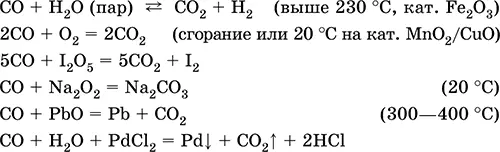
Получение в промышленности: сжигание кокса (см.) при недостатке кислорода, восстановление раскаленным коксом углекислого газа и водяного пара:

Диоксид углерода СO 2.Кислотный оксид. Техническое название — углекислый газ. Бесцветный газ, без запаха, в 1,5 раза тяжелее воздуха (можно «переливать» из сосуда в сосуд). Молекула неполярна, имеет линейное строение [С(O) 2] (sр-гибридизация), содержит ковалентные σπ-связи С=O. Термически устойчив до температуры красного каления. При сжатии (давление = 50 атм) и охлаждении легко переходит в жидкое и твердое («сухой лед») состояния.
Твердый СO 2возгоняется уже при низких температурах. Мало растворим в воде (O,88 л/1 л Н 2O при 20 °C); образует моногидрат, который медленно изомеризуется (на 0,4 %) в угольную кислоту. Реагирует со щелочами. Восстанавливается магнием и кальцием. Из воздуха удаляется при контакте с пероксидом натрия (одновременно регенерируется кислород).
Простейшая качественная реакция – угасание горящей древесной лучинки в атмосфере СO 2.
Применяется в многотоннажных производствах соды, сахара и карбамида, в пищевой промышленности для газирования безалкогольных напитков и как хладагент.
Содержится в воздухе (0,03 % по объему), воде минеральных источников. Не поддерживает горение и дыхание. Ассимилируется зелеными растениями при фотосинтезе (с помощью хлорофилла и под воздействием солнечных лучей). Ядовит при содержании в воздухе свыше 15 % по объему.
Уравнения важнейших реакций:

Получение в промышленности– при полном сгорании кокса (см.) или при обжиге известняка:
СаСO 3= СаО + СO 2 (900—1200 °C)
в лаборатории– при обработке карбонатов (например, кусочков мрамора СаСO 3) сильными кислотами:
СаСO 3(т)+ H 2SO 4= CaSO 4↓ + Н 2O + CO 2↑
7.5.3. Карбонаты
Карбонат натрия Na 2CO 3.Оксосоль. Техническое название кальцинированная сода. Белый, при нагревании плавится и разлагается. Чувствителен к влаге и углекислому газу в воздухе. Образует декагидрат ( кристаллическая сода). Хорошо растворим в воде, гидролизуется по аниону, создает в растворе сильнощелочную среду. Разлагается сильными кислотами. Восстанавливается коксом. Вступает в реакции ионного обмена.
Качественная реакция на ион СО 3 2-– образование белого осадка карбоната бария, разлагаемого сильными кислотами (НCl, HNO 3) с выделением углекислого газа.
Применяется для синтеза соединений натрия, устранения «постоянной» жесткости пресной воды, в производстве стекла, мыла и других моющих средств, целлюлозы, минеральных красок, эмалей. В природе содержится в грунтовых рассолах, рапе соляных озер.
Уравнения важнейших реакций:
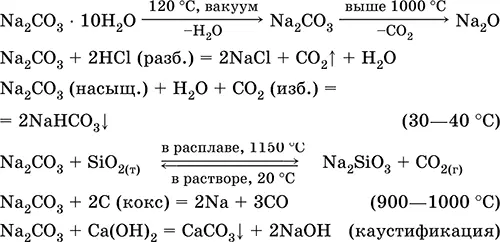
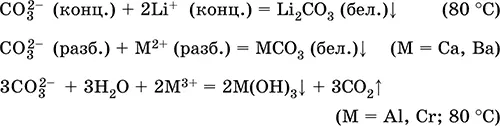
Получение в промышленности( способ Сольве, 1861–1863):
а) через насыщенный раствор NaCl пропускают смесь NH 3и СO 2:
NaCl + NH 3+ Н 2O + СO 2= NH 4Cl + NaHCO 3↓
(в этих условиях питьевая сода малорастворима);
б) осадок NaHCO 3подвергают обезвоживанию ( кальцинированию):
2NaHCO 3= Na 2CO 3+ Н 2O + СO 2
Карбонат калия К 2СO 3.Оксосоль. Техническое название поташ. Белый, гигроскопичный. Плавится без разложения, при дальнейшем нагревании разлагается. Чувствителен к влаге и углекислому газу в воздухе. Очень хорошо растворим в воде, гидролизуется по аниону, создает в растворе сильнощелочную среду. Разлагается сильными кислотами. Вступает в реакции ионного обмена.
Применяется в производстве оптического стекла, жидкого мыла, минеральных красок, многих соединений калия, как дегидратирующий агент.
Уравнения важнейших реакций:
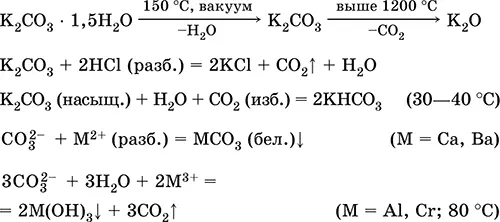
Получение в промышленности:
а) нагревание сульфата калия [природное сырье – минералы каинит KMg(SO 4)Cl ЗН 2O и шёнит K 2Mg(SO 4) 2 • 6Н 2O] с гашёной известью Са(ОН) 2в атмосфере СО (давление = 15 атм):
K 2SO 4+ Са(ОН) 2+ 2СО = 2K(HCOO) + CaSO 4
б) прокаливание формиата калия К(НСОО) на воздухе:
2K(HCOO) + O 2= К 2СO 3+ Н 2O + СO 2
Гидрокарбонат натрия NaHCO 3.Кислая оксосоль. Техническое название питьевая сода. Белый рыхлый порошок. При слабом нагревании разлагается без плавления, во влажном состоянии начинает разлагаться при комнатной температуре. Умеренно растворим в воде, гидролизуется по аниону в небольшой степени. Разлагается кислотами, нейтрализуется щелочами. Вступает в реакции ионного обмена.
Качественная реакция на ион НСОд – образование белого осадка карбоната бария при действии баритовой воды и разложение осадка сильными кислотами (НCl, HNO 3) с выделением углекислого газа. Применяется в пищевой промышленности, как лекарственное средство.
Уравнения важнейших реакций:
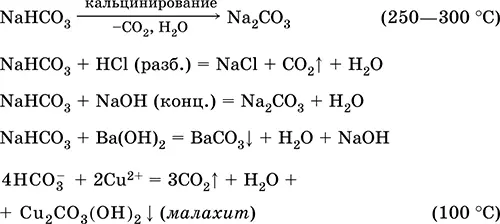
Получение : насыщение раствора Na 2CO 3(см.) углекислым газом.
Карбонат кальция СаСO 3.Оксосоль. Распространенное природное вещество, главная составная часть осадочной горной породы – известняка (его разновидности – мел, мрамор, известковый туф, мергель), чистый СаСO 3в природе – это минерал кальцит. Белый, при прокаливании разлагается, плавится под избыточным давлением СO 2. Нерастворим в воде (= 0,0007 г/100 г Н 2O).
Реагирует с кислотами, солями аммония в горячем растворе, коксом. Переводится в раствор действием избытка углекислого газа с образованием гидрокарбоната Са(НСO 3) 2(существует только в растворе), который определяет «временную» жесткость пресной воды (вместе с солями магния и железа). Устранение жесткости (умягчение воды) проводится кипячением или нейтрализацией гашёной известью.
Читать дальшеИнтервал:
Закладка:










