Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Красный фосфор состоит из полимерных молекул Р nразной длины. Аморфный, при комнатной температуре медленно переходит в белый фосфор. При нагревании до 416 °C возгоняется (при охлаждении пара конденсируется белый фосфор). Нерастворим в органических растворителях. Химическая активность ниже, чем у белого фосфора. На воздухе загорается только при нагревании.
Применяется как реагент (более безопасный, чем белый фосфор) в неорганическом синтезе, наполнитель ламп накаливания, компонент намазки коробка при изготовлении спичек. Не ядовит.
Белый фосфор состоит из молекул Р 4. Мягкий как воск (режется ножом). Плавится и кипит без разложения (t пл44,14 °C, t кип287,3 °C, ρ 1,82 г/см 3). Окисляется на воздухе (зеленое свечение в темноте), при большой массе возможно самовоспламенение. В особых условиях переводится в красный фосфор. Хорошо растворим в бензоле, эфирах, сероуглероде. Не реагирует с водой, хранится под слоем воды. Чрезвычайно химически активен. Проявляет окислительно-восстановительные свойства. Восстанавливает благородные металлы из растворов их солей.
Применяется в производстве Н 3РO 4и красного фосфора, как реагент в органических синтезах, раскислитель сплавов, зажигательное средство. Горящий фосфор следует гасить песком (но не водой!). Чрезвычайно ядовит.
Уравнения важнейших реакций:
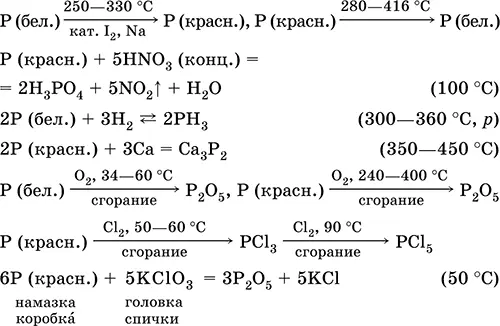
Получение в промышленности– восстановление фосфорита раскаленным коксом (песок добавляют для связывания кальция):
Са 3(РO 4) 2+ 5С + 3SiO 2= 3CaSiO 3+ 2 Р+ 5СО (1000 °C)
Пар фосфора охлаждают и получают твердый белый фосфор.
Красный фосфор готовят из белого фосфора (см. выше), в зависимости от условий степень полимеризации n (Р n) может быть различной.
Фосфин РН 3.Бинарное соединение, степень окисления фосфора равна – III. Бесцветный газ с неприятным запахом. Молекула имеет строение незавершенного тетраэдра [: Р(Н) 3] (sр 3-гибридизация). Мало растворим в воде, не реагирует с ней (в отличие от NH 3). Сильный восстановитель, сгорает на воздухе, окисляется в HNO 3(конц.). Присоединяет HI. Применяется для синтеза фосфорорганических соединений. Сильно ядовит.
Уравнения важнейших реакций:
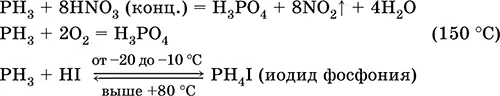
Получение в лаборатории:
Са 3Р 2+ 6НCl (разб.) = ЗСаCl 2+ 2 РН 3↑
Оксид фосфора (V) Р 2O 5.Кислотный оксид. Белый, термически устойчивый. В твердом и газообразном состояниях димер Р 4О 10со строением из четырех тетраэдров [O=Р(O) 3], связанных по трем вершинам (Р – О—Р). При очень высоких температурах мономеризуется до Р 2O 5. Существует также стеклообразный полимер (Р 2O 5) n. Чрезвычайно гигроскопичен, энергично реагирует с водой, щелочами. Восстанавливается белым фосфором. Отнимает воду у кислородсодержащих кислот.
Применяется как весьма эффективный дегидратирующий агент для осушения твердых веществ, жидкостей и газовых смесей, реагент в производстве фосфатных стекол, катализатор полимеризации алкенов. Ядовит.
Уравнения важнейших реакций:
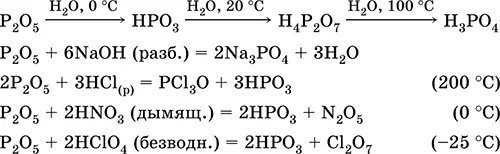
Получение : сжигание фосфора (см.) в избытке сухого воздуха.
Ортофосфорная кислота Н 3РO 4.Оксокислота. Белое вещество, гигроскопичное, конечный продукт взаимодействия Р 2O 5с водой. Молекула имеет строение искаженного тетраэдра [Р(O)(OН) 3] (sр 3-гибридизация), содержит ковалентные σ-связи Р – ОН и σ, π-связь Р=O. Плавится без разложения, при дальнейшем нагревании разлагается. Хорошо растворяется в воде (548 г/100 г Н 2O). Слабая кислота в растворе, нейтрализуется щелочами, не полностью – гидратом аммиака. Реагирует с типичными металлами. Вступает в реакции ионного обмена.
Качественная реакция – выпадение желтого осадка ортофосфата серебра (I). Применяется в производстве минеральных удобрений, для осветления сахарозы, как катализатор в органическом синтезе, компонент антикоррозионных покрытий на чугуне и стали.
Уравнения важнейших реакций:

Получение в промышленности: кипячение фосфоритной руды в серной кислоте:
Са 3(РO 4) 2+ 3H 2SO 4(конц.) = 2 Н 3РO 4+ 3CaSO 4↓
Ортофосфат натрия Na 3PO 4.Оксосоль. Белый, гигроскопичный. Плавится без разложения, термически устойчивый. Хорошо растворим в воде, гидролизуется по аниону, создает в растворе сильнощелочную среду. Реагируется в растворе с цинком и алюминием. Вступает в реакции ионного обмена.
Качественная реакция на ион РO 4 3-– образование желтого осадка ортофосфата серебра (I).
Применяется для устранения «постоянной» жесткости пресной воды, как компонент моющих средств и фотопроявителей, реагент в синтезе каучука. Уравнения важнейших реакций:
Na 3PO 412Н 2O = Na 3PO 4+ 12Н 2O (200 °C, вакуум)
2РО 4 3-(конц.) + 8Н 2O + 2Al = 2[Al(ОН) 4] -+ 2НРО 4 2-+ ЗН 2↑
2РО 4 3-(конц.) + 4Н 2O + Zn = [Zn(OH) 4] 2-+ 2HPO 4 2-+ Н 2↑
2РО 4 3-(разб.) + ЗСа 2+= Са 3(РO 4) 2↓
РО 4 3-(разб.) + 3Ag += Ag 3PO 4↓ (желт.)↓
Получение : полная нейтрализация Н 3РO 4(см.) гидроксидом натрия или по реакции:
2Н 3РO 4+ 3Na 2CO 3= 2 Na 3PO 4+ 3CO 2↑ + 3H 2O
Гидроортофосфат натрия Na 2HPO 4.Кислая оксосоль. Белый, при умеренном нагревании разлагается без плавления. Хорошо растворим в воде, гидролизуется по аниону. Реагирует с Н 3РO 4(конц.), нейтрализуется щелочами. Вступает в реакции ионного обмена.
Качественная реакция на ион НРО 4 2-– образование желтого осадка ортофосфата серебра (I).
Применяется как эмульгатор при сгущении коровьего молока, компонент пищевых пастеризаторов и фотоотбеливателей.
Уравнения важнейших реакций:
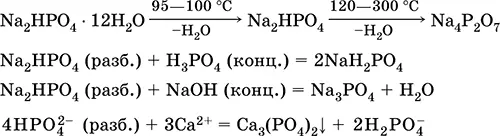
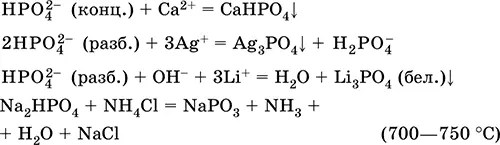
Получение : неполная нейтрализация Н 3РO 4гидроксидом натрия в разбавленном растворе:
2NaOH + Н 3РO 4= Na 2HPO 4+ 2Н 2O
Дигидроортофосфат натрия NaH 2PO 4.Кислая оксосоль. Белый, гигроскопичный. При умеренном нагревании разлагается без плавления. Хорошо растворим в воде, анион Н 2РO 4подвергается обратимой диссоциации. Нейтрализуется щелочами. Вступает в реакции ионного обмена.
Качественная реакция на ион Н 2РO 4– образование желтого осадка ортофосфата серебра(I).
Применяется в производстве стекла, для защиты стали и чугуна от коррозии, как умягчитель воды.
Читать дальшеИнтервал:
Закладка:










