Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ
- Название:Химия. Полный справочник для подготовки к ЕГЭ
- Автор:
- Жанр:
- Издательство:Array Array
- Год:2009
- Город:Москва
- ISBN:978-5-17-060638-2, 978-5-271-24368-4
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Ростислав Лидин - Химия. Полный справочник для подготовки к ЕГЭ краткое содержание
Теоретический материал изложен в краткой, доступной форме. Каждый раздел сопровождается примерами тестовых заданий, позволяющими проверить свои знания и степень подготовленности к аттестационному экзамену. Практические задания соответствуют формату ЕГЭ. В конце пособия приводятся ответы к тестам, которые помогут школьникам и абитуриентам проверить себя и восполнить имеющиеся пробелы.
Пособие адресовано старшим школьникам, абитуриентам и учителям.
Химия. Полный справочник для подготовки к ЕГЭ - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
Применяется для производства СаО, СO 2, цемента, стекла и минеральных удобрений [в том числе известковой селитры Ca(NO 3) 24Н 2O], как наполнитель бумаги и резины, строительный камень (щебень) и компонент бетона и шифера, в виде осажденного порошка – для изготовления школьных мелков, зубных порошков и паст, смесей для побелки помещений.
Уравнения важнейших реакций:
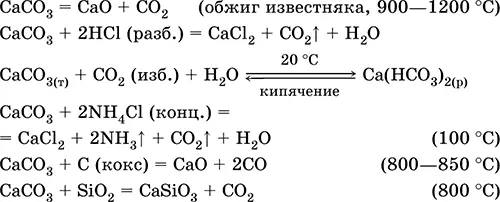
7.5.4. Кремний
Кремний – элемент 3-го периода и IVA-группы Периодической системы, порядковый номер 14. Электронная формула атома [ 10Ne]3s 23p 2. Характерная степень окисления в соединениях +IV.
Шкала степеней окисления кремния:
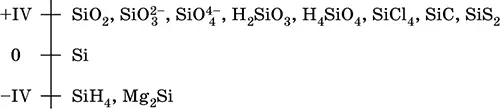
Электроотрицательность кремния невысока для неметаллов (2,25). Проявляет неметаллические (кислотные) свойства; образует оксиды, кремниевые кислоты, очень большое число солей – силикатов в виде цепей, лент и трехмерных сеток тетраэдров [SiO 4], бинарные соединения. В настоящее время широко развивается химия органических соединений кремния со связями Si – С и кремнийорганических полимеров – силиконов и силиконовых каучуков со связями Si – Si, Si – О и Si – С.
Важнейший элемент неживой природы, второйпо химической распространенности. Встречается только в связанном виде. Жизненно важный элемент для многих организмов.
Кремний Si.Простое вещество. Крупнокристаллический – темно-серый, с металлическим блеском, весьма твердый, очень хрупкий, непрозрачный, тугоплавкий, распространенный полупроводник. Кристаллическая решетка – атомная, связи Si – Si очень прочные. Аморфный – белый или желто-коричневый (с примесями, в основном Fe), химически более активен. Устойчив на воздухе (покрыт прочной оксидной пленкой), не реагирует с водой. Реагирует с HF (конц.), щелочами. Окисляется кислородом, хлором. Восстанавливается магнием. Спекается с графитом. Промышленно важным является сплав с железом – ферросилиций (12–90 % Si). Применяется как легирующая добавка в стали и сплавы цветных металлов, компонент полупроводниковых материалов для микроэлектроники, основа силиконов.
Уравнения важнейших реакций:
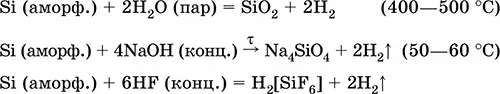

Получение в промышленности: восстановление SiCl 4или SiO 2при прокаливании:
SiCl 4+ 2Zn = Si+ 2ZnCl 2
SiO 2+ 2Mg = Si+ 2MgO
(последняя реакция может быть осуществлена и в лаборатории, после обработки соляной кислотой остается аморфный кремний).
Диоксид кремния SiO 2.Кислотный оксид. Белый порошок (кварцевый песок) и прозрачные кристаллы, природный продукт окрашен примесями (кремнезём) – в виде обычного песка и камня (кремень). Кристаллическая решетка атомная, каждый атом кремния окружен четырьмя атомами кислорода [Si(O) 4], а каждый атом кислорода – двумя атомами кремния [O(Si) 2]. Имеет несколько кристаллических модификаций (все минералы), важнейшие — кварц, тридимит и кристобалит, редко встречающиеся и искусственно полученные — китит, коэсит, стишовит, меланофлогит, волокнистый кремнезём. Тугоплавкий, при медленном охлаждении расплава образуется аморфная форма – кварцевое стекло (в природе минерал лешательеит). Наиболее химически активна аморфная форма.
Практически не реагирует с водой (из раствора осаждается гидрат SiO 2nН 2O), распространенными кислотами. Кварцевое стекло разъедается в HF (конц.). Реагирует со щелочами в растворе (образует ортосиликаты) и при сплавлении (продукты — метасиликаты). Легко хлорируется в присутствии кокса. Восстанавливается коксом, магнием, железом (в доменном процессе).
Применяется как промышленное сырье в производстве кремния, обычного, термо– и химически стойкого стекла,
фарфора, керамики, абразивов и адсорбентов, наполнитель резины, смазок, клеев и красок, компонент строительных связующих растворов, в виде монокристаллов кварца – основа генераторов ультразвука и точного хода кварцевых часов. Разновидности кварца ( горный хрусталь, розовый кварц, аметист, дымчатый кварц, халцедон, оникс и др.) – драгоценные, полудрагоценные или поделочные камни.
Уравнения важнейших реакций:

Полигидрат диоксида кремния SiO 2nH 2O.Кремниевые кислоты с переменным содержанием SiO 2и Н 2O. Белый, аморфный (стекловидный) полимер с цепочечным, ленточным, листовым, сетчатым и каркасным строением. При нагревании постепенно разлагается. Очень мало растворим в воде. Над осадком в растворе существует мономерная слабая ортокремниевая кислота H 4SiO 4(тетраэдрическое строение, sр 3-гибридизация), растворимость 0,00673 г/100 г Н 2O при 20 °C. При стоянии раствора идет поликонденсация и медленно образуются вначале кремниевые кислоты H 6Si 2O 7, H 2Si 2O 5, H 10Si 2O 9, затем гидрозоль [H 2SiO 3] n(золь метакремниевой кислоты) и, наконец, гидрогель SiO 2 • nН 2O (n < 2). При высушивании гидрогель переходит в силикагель SiO 2 • nН 2O (n < 1). Скорость гелеобразования максимальна в слабокислотной среде.
Переводится в раствор действием концентрированных щелочей. По остальным химическим свойствам подобен SiO 2. В природе – минералы опал и халцедон (агат, яшма). Мономерная метакремниевая кислота H 2SiO 3не получена.
Уравнения важнейших реакций:
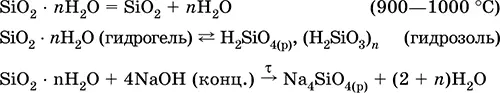
Получение : вытеснение сильной кислотой из раствора силиката, например:
K 2SiO 3+ 2НCl + (n – 1) Н 2O = 2КCl + SiO 2nН 2O↓
Метасиликат натрия Na 2SiO 3.Оксосоль. Белый, при нагревании плавится без разложения. Растворяется в холодной воде (сильный гидролиз по аниону). Концентрированный раствор – коллоидный («жидкое стекло», содержит гидрозоль SiO 2nН 2O). Разлагается в горячей воде, реагирует с кислотами, щелочами, углекислым газом.
Применяется как компонент шихты в производстве стекла, специальных цементов и бетонов, входит в состав силикатных красок и клея, холодных глазурей, алюмосиликатных катализаторов, при изготовлении бумаги и картона, силикагеля, синтетических цеолитов. Уравнения важнейших реакций:
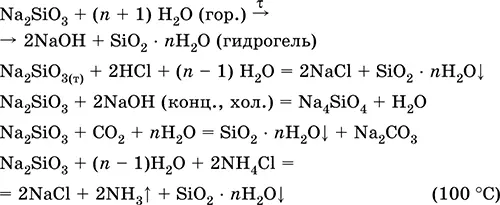
Получение : сплавление соды с песком
Читать дальшеИнтервал:
Закладка:










