Эрик Роджерс - Физика для любознательных. Том 3. Электричество и магнетизм. Атомы и ядра
- Название:Физика для любознательных. Том 3. Электричество и магнетизм. Атомы и ядра
- Автор:
- Жанр:
- Издательство:Мир
- Год:1973
- Город:Москва
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Эрик Роджерс - Физика для любознательных. Том 3. Электричество и магнетизм. Атомы и ядра краткое содержание
Физика для любознательных. Том 3. Электричество и магнетизм. Атомы и ядра - читать онлайн бесплатно полную версию (весь текст целиком)
Интервал:
Закладка:
При изменении расстояния х между электроном и ядром на величину d x из электрической потенциальной энергии в кинетическую энергию передается величина
F∙d x, или
Это уменьшение потенциальной энергии атома, т. е. энергия, реализованная из накопленного запаса. (Здесь эта величина положительна, поскольку как F , так и d x отрицательны: F — притяжение внутрь , a d x — смещение внутрь , уменьшение х .) Очевидно, наибольшую потенциальную энергию электрон имел на бесконечности, когда его отвели наиболее далеко от притягивающего ядерного заряда, и он по дороге туда накопил потенциальную энергию. Поэтому, если считать потенциальную энергию электрона на бесконечности равной нулю, то вблизи ядра она должна быть отрицательной.
Потенциальная энергия электрона, перенесенного из бесконечности на орбиту радиусом r , равна
что после интегрирования дает
0 — ∙( e)∙(Z e)/ r
Таким образом, потенциальная энергия электрона равна
П.Э.= — ∙( e)∙(Z e)/ r
Поскольку при орбитальном движении
— mv 2/ r= ∙(- e)∙(Z e)/ r 2 (знак минус показывает направление силы внутрь),
то
П.Э.= — ∙( e)∙(Z e)/ r = — mv 2= — (2 x К.Э.)
Полная энергия
Е= К.Э.+ П.Э.= 1/ 2 mv 2 + (— mv 2) = — 1/ 2 mv 2
Нам нужно знать выражение для энергии Е (через квантовое число n и другие постоянные), не содержащее v или r . Воспользуемся соотношением для орбитального движения
— mv 2/ r= ∙(- e)∙(Z e)/ r 2
и исключим r с помощью квантового правила mv∙2π r= nh:
mv 2 = ∙( e)∙(Z e)/ r
mv = nh/2π r
Разделив первое равенство на второе, получим
v = ∙( e)∙(Z e)∙(2π)/ nh
Тогда
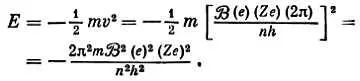
Подставим n = n iдля начального и n = n fдля конечного уровней, между которыми переходит электрон, и получим
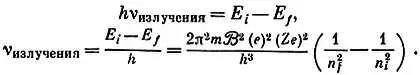
Откуда спектроскопическая постоянная
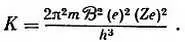
При подстановке измеренных значений е, e / m, h , и для водорода Z = 1 эта формула дает превосходное согласие с величиной K , полученной экспериментально из измерений спектров, а именно 3,286∙10 15в сравнении с 3,290∙10 15.
Дальнейшие предсказания
Предсказания Бора можно продолжить. Предположим, атом гелия потерял один из двух своих электронов, а оставшийся электрон испускает свет при переходе между орбитами. Тогда ионизованный атом гелия с одним оставшимся электроном подобен атому водорода с двойным зарядом ядра +2 е . Для Z = 2 предсказываемые частоты излучения ровно в 4 раза больше частот излучения водорода (см. формулу Бора для К ). Такие линии были уже открыты в спектре гелия при искровом разряде и ошибочно приписывались водороду в каком-то необычном состоянии. Бор не только указал, что они исходят от однократно ионизованного гелия, но, используя входящую в предсказание малую поправку на конечность массы ядра, оценил отношение массы электрона к массе протона и получил 1/1830.
Кроме того, формула Бора для водорода, примененная к переходам внутренних электронов в тяжелых атомах, предсказывает частоту рентгеновского излучения, которая много больше частоты видимого света, поскольку постоянная К содержит [196]множитель Z 2. Это позволило Мозли сравнить атомные номера ( Z ) различных элементов, находя квадратный корень из частоты рентгеновского излучения от соответствующей мишени. Это был первый простой способ измерения атомных номеров. Атомы любого элемента могут излучать несколько серий, причем формулы, связывающие частоты соответствующих линий из разных серий имеют вид арифметических разностей. Бор сразу объяснил эти соотношения, приписав все спектральные линии переходам с одних энергетических уровней на другие. Каждая серия относится к определенному конечному уровню энергии. Тогда вычитание частоты одной линии из другой дает разность между энергиями двух верхних уровней, и эту разность можно получить несколькими вычитаниями (фиг. 197). Бор смог также вычислить «энергию ионизации» атома водорода, т. е. энергию, необходимую для полного удаления электрона из атома. По его предсказаниям эта величина равна 13,54 эв [197]. Трудный эксперимент — бомбардировка атомарного водорода электронами — дал значение 13,6 эв.
Используя измеренные спектры частот рентгеновского излучения и видимого света, Бор изобразил энергетические уровни атомов всех элементов и построил схему строения атома, объясняющую периодическую систему химических элементов. В его схеме электроны вращаются по определенным окружностям (или эллипсам), образующим группы, или оболочки. Это была довольно удачная схема. Она «объяснила» общие химические свойства элементов и даже предсказала свойства одного неизвестного элемента и помогла его открыть (речь идет о гафнии).
Плодотворность теории подтвердила объявленные Бором правила; но они оставались произвольными правилами без обоснований.
Фиг. 197. Уровни энергии в воровской модели атома (упрощенно).
Основа уверенности Бора . Принцип соответствия
Все же эти правила были не совсем произвольными, поскольку Бор прежде всего сохранил надежную связь с прежней теорией. Рассмотрим некоторый предельный случай, когда квантовые ограничения становятся несущественными. Здесь предсказания, которые делает новая теория, должны совпадать с предсказаниями старой, классической теории. В тех местах, где старый теоретический материал оказывается непригодным при объяснении фактов, его нужно вырезать; но новый материал, который используется для того, чтобы залатать брешь или расширить целое изделие, на краях должен вплетаться в старую ткань.
Принцип соответствия: в той области, где различия между предположениями старой и новой теории несущественны, обе теории должны перекрываться и находиться в согласии друг с другом . Такое утверждение кажется очевидным, но оно служит мощным направляющим правилом для новых предположений. Это общее правило подойдет для любой науки, для каждой хорошей теории.
Читать дальшеИнтервал:
Закладка:








