Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
У серы и у остальных элементов подгруппы число неспаренных электронов в атоме может быть увеличено путем перевода s- и р-электронов на d-подуровень внешнего слоя. В связи с этим указанные элементы проявляют ковалентность, равную не только 2, но также 4 и 6.
Все элементы данной подгруппы, кроме полония, неметаллы, хотя и менее активные, чем галогены. В своих соединениях они проявляют как отрицательную, так и положительную окисленность. В соединениях с металлами и с водородом их степень окисленности, как правило, равна —2. В соединениях с неметаллами, например с кислородом, она может иметь значение +4 или +6. Исключение при этом составляет сам кислород. По величине электроотрицательности он уступает только фтору (см. табл. 6 на стр. 118); поэтому только в соединении с этим элементом (OF 2) его окисленность положительна (+2). В соединениях со всеми другими элементами окисленность кислорода отрицательна и обычно равна —2. В пероксиде водорода и его производных (см. § 117) она равна —1.
Как и в группе галогенов, физические и химические свойства рассматриваемых элементов закономерно изменяются с увеличением порядкового номера. Появление новых электронных слоев влечет за собой увеличение радиусов атомов, уменьшение электроотрицательности, понижение окислительной активности незаряженных атомов и усиление восстановительных свойств атомов со степенью окисленности —2.
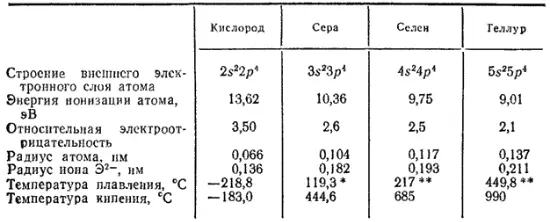
Таблица 25. Некоторые свойства кислорода и его аналогов
- 361 -
Поэтому неметаллические свойства, ярко выраженные у кислорода, оказываются очень ослабленными у теллура.
Некоторые свойства элементов главной подгруппы шестой группы приведены в табл. 25.
КИСЛОРОД (OXYGENIUM)
123. Кислород в природе. Воздух.
Кислород — самый распространенный элемент земной коры. В свободном состоянии он находится в атмосферном воздухе, в связанном виде входит в состав воды, минералов, горных пород и всех веществ, из которых построены организмы растений и животных. Массовая доля кислорода в земной коре составляет около 47%.
Природный кислород состоит из трех стабильных изотопов: 16O(99.76%) и 18O(0.2%).
Атмосферный воздух представляет собой смесь многих газов. Кроме кислорода и азота, образующих основную массу воздуха, в состав его входят в небольшом количестве благородные газы, диоксид углерода и водяные пары. Помимо перечисленных газов, в воздухе содержится еще большее или меньшее количество пыли и некоторые случайные примеси. Кислород, азот и благородные газы считаются постоянными составными частями воздуха, так как их содержание в воздухе практически повсюду одинаково. Содержание же диоксида углерода, водяных паров и пыли может изменяться в зависимости от условий.
Диоксид углерода образуется в природе при горении дерева и угля, дыхании животных, гниении. Особенно много CO 2как продукта сжигания огромных количеств топлива поступает в атмосферу в больших промышленных центрах.
В некоторых местах земного шара CO 2выделяется в воздух вследствие вулканической деятельности, а также из подземных источников. Несмотря на непрерывное поступление диоксида углерода в атмосферу, содержание его в воздухе довольно постоянно и составляет в среднем около 0..3%(об). Это объясняется поглощением диоксида углерода растениями, а также его растворением в воде.
Водяные пары могут находиться в воздухе в различных количествах. Содержание их колеблется от долей процента до нескольких процентов и зависит от местных условий и от температуры.
Пыль, находящаяся в воздухе, состоит главным образом из мельчайших частиц минеральных веществ, образующих земную кору, частичек угля, пыльцы растений, а также различных бактерий. Количество пыли в воздухе очень изменчиво: зимой ее меньше, летом больше.
- 362 -
После дождя воздух становится чище, так как капли дождя увлекают с собой пыль.
Наконец, к случайным примесям воздуха относятся такие вещества, как сероводород и аммиак, выделяющиеся при гниении органических остатков; диоксид серы SO 2, получающийся при обжиге сернистых руд или при горении угля, содержащего серу; оксиды азота, образующиеся при электрических разрядах в атмосфере, и т. п. Эти примеси обычно встречаются в ничтожных количествах и постоянно удаляются из воздуха, растворяясь в дождевой воде.
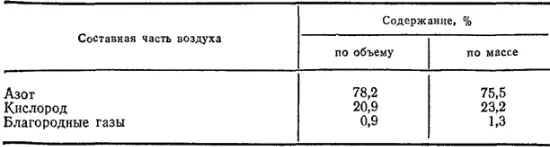
Если учитывать только постоянные составные части воздуха, то его состав можно выразить данными, приведенными в табл. 26.
Таблица 26. Состав воздуха
Масса 1 л воздуха при 20°C и нормальном атмосферном давлении равна 1,293 г. При температуре -140°C и давлении около 4 МПа воздух конденсируется в бесцветную прозрачную жидкость.
Несмотря на низкую при обычном давлении температуру кипения (около -190°C), жидкий воздух можно довольно долго сохранять в сосудах Дьюара — стеклянных сосудах с двойными стенками, из пространства между которыми воздух откачан (рис. 109).
В жидком воздухе легко переходят в твердое состояние этиловый спирт, диэтиловый эфир и многие газы. Если, например, пропускать через жидкий воздух диоксид углерода, то он превращается в белые хлопья, похожие по внешнему виду на снег. Ртуть, погруженная в жидкий воздух, становится твердой и ковкой.
Многие вещества, охлажденные жидким воздухом, резко изменяют свои свойства. Так, цинк и олово становятся настолько хрупкими, что легко превращаются в порошок, свинцовый колокольчик издает чистый звенящий звук, а замороженный резиновый мячик разбивается вдребезги, если уронить его на пол.
Поскольку температура кипения кислорода (-183°C) лежит выше, чем температура кипения азота (-195,8°C) , то кислород легче превращается в жидкость, чем азот.
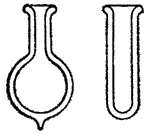
Рис. 109. Сосуды Дьюара (в разрезе).
- 363 -
Поэтому жидкий воздух богаче кислородом, чем атмосферный. При хранении жидкий воздух еще больше обогащается кислородом вследствие преимущественного испарения азота.
Жидкий воздух производят в больших количествах. Он используется главным образом для получения из него кислорода, азота и благородных газов; разделение производят путем ректификации — дробной перегонки.
124. Получение и свойства кислорода.
Кислород был впервые получен в чистом виде К. В. Шееле в 1772 г., а затем в 1774 г. Д. Пристли (Англия), который выделил его из оксида ртути(II). Однако Пристли не знал, что полученный им газ входит в состав воздуха. Только спустя несколько лет Лавуазье, подробно изучивший свойства этого газа, установил, что он является составной частью воздуха.
Читать дальшеИнтервал:
Закладка:








