Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
Отдельные слои атомов в кристалле графита, связанные между собой сравнительно слабо, легко отделяются друг от друга.
Этим объясняется малая механическая прочность графита. Если провести куском графита по бумаге, то мельчайшие кристаллики графита, имеющие вид чешуек, прилипают к бумаге, оставляя на ней серую черту. На этом основано применение графита для изготовления карандашей.
На воздухе графит не загорается даже при сильном накаливании, но легко сгорает в чистом кислороде, превращаясь в диоксид углерода.
Благодаря электрической проводимости графит применяется для изготовления электродов. Из смеси графита с глиной делают огнеупорные тигли для плавления металлов. Смешанный с маслом графит служит прекрасным смазочным средством, так как чешуйки его, заполняя неровности материала, создают гладкую поверхность, облегчающую скольжение. Графит применяют также в качестве замедлителя нейтронов в ядерных реакторах.
Кроме природного, в промышленности находит применение искусственный графит. Его получают главным образом из лучших сортов каменного угля. Превращение происходит при температурах около 3000°C в электрических печах без доступа воздуха. На основе естественного и, особенно, искусственного графита изготовляют материалы, применяемые в химической промышленности. Благодаря их высокой химической стойкости они используются для футеровки, изготовления труб и др.
Графит термодинамически устойчив в широком интервале температур и давлений, в частности при обычных условиях. В связи с этим при расчетах термодинамических величин в качестве стандартного состояния углерода принимается графит. Алмаз термодинамически устойчив лишь при высоких давлениях (выше 10 9Па). Однако скорость превращения алмаза в графит становится заметной лишь при температурах выше 1000°C при 1750°C превращение алмаза в графит происходит быстро.
«Аморфный» углерод (уголь). При нагревании углеродсодержащих соединений без доступа воздуха из них выделяется черная масса, называемая «аморфным» углеродом или просто углем. Такой углерод состоит из мельчайших кристалликов с разупорядоченной структурой графита. Уголь растворяется во многих расплавленных металлах, например в железе, никеле, платине. Плотность угля колеблется от 1,8 до 2,1 г/см 3.
Угли существенно различаются по своим свойствам в зависимости от вещества, из которого они получены и способа получения. Кроме того, они всегда содержат примеси, сильно влияющие на их свойства. Важнейшие технические сорта угля: кокс, древесный уголь, костяной уголь и сажа.
Кокс получается при сухой перегонке каменного угля. Применяется он главным образом в металлургии при выплавке металлов из руд.
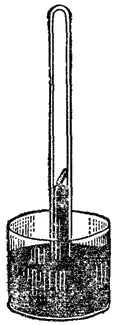
Рис. 119. Прибор для демонстрации поглощения аммиака углем.
Древесный уголь получается при нагревании дерева без доступа воздуха. При этом улавливают ценные продукты сухой перегонки — метиловый спирт, уксусную кислоту и др. Древесный уголь применяется в металлургической промышленности, в кузнечном деле.
Благодаря пористому строению, древесный уголь обладает высокой адсорбционной способностью.
Чтобы наблюдать адсорбцию газов углем, произведем следующий опыт. Наполним аммиаком стеклянный цилиндр и опустим открытый конец его в чашку с ртутью (рис. 119). Затем, прокалив на горелке кусочек древесного угля, погрузим его в ртуть и подведем под отверстие цилиндра с аммиаком. Уголь всплывает на поверхность ртути в цилиндре, и ртуть сейчас же начинает подниматься вверх вследствие поглощения аммиака углем.
Особенно хорошо поглощают газы активные угли (стр. 312). Они применяются для поглощения паров летучих жидкостей из воздуха и газовых смесей, в противогазах, а также в качестве катализатора в некоторых химических производствах.
Уголь обладает способностью адсорбировать не только газы, но и растворенные вещества. Это его свойство открыл в конце XVIII века русский академик Т. Е. Ловиц.
Костяной уголь получается путем обугливания обезжиренных костей. Он содержит от 7 до 11% углерода, около 80% фосфата кальция и другие соли. Костяной уголь отличается очень большой поглотительной способностью, особенно по отношению к органическим красителям, и служит для удаления из растворов различных красящих веществ.
Сажа представляет собой наиболее чистый «аморфный» углерод. В промышленности ее получают термическим разложением метана, а также сжиганием при недостаточном доступе воздуха смолы, скипидара и других богатых углеродом веществ. Сажа применяется в качестве черной краски (тушь, типографская краска), а также в производстве резины как ее составная часть.
154. Химические свойства углерода. Карбиды.
При низких температурах и уголь, и графит и, в особенности, алмаз инертны. При нагревании их активность увеличивается: уголь легко соединяется с кислородом и служит хорошим восстановителем. Важнейший процесс металлургии — выплавка металлов из руд — осуществляется путем восстановления оксидов металлов углем (или монооксидом углерода).
С кислородом углерод образует диоксид (или двуокись) углерода CO 2, часто называемый также углекислым газом, и оксид углерода(II), или монооксид углерода, СО.
При очень высоких температурах углерод соединяется с водородом, серой, кремнием, бором и многими металлами; уголь вступает в реакции легче, чем графит и тем более алмаз.
Соединения углерода с металлами и другими элементами, которые по отношению к углероду являются электроположительными, называются карбидами. Их получают прокаливанием металлов или их оксидов с углем.
Карбиды — кристаллические тела. Природа химической связи в них может быть различной. Так, многие карбиды металлов главных подгрупп I, II и III групп периодической системы представляют собой солеобразные соединения с преобладанием ионной связи. К их числу относятся карбиды алюминия Al 4C 3и кальция CaC 2. Первый из них можно рассматривать как продукт замещения водорода на металл в метане CH 4, а второй — в ацетилене C 2H 2. Действительно, при взаимодействии карбида алюминия с водой образуется метан
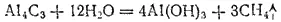
а при взаимодействии с водой карбида кальция — ацетилен:
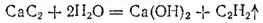
В карбидах кремния SiC (см. § 178) и бора B 4C связь между атомами ковалентная. Эти вещества характеризуются высокой твердостью, тугоплавкостью, химической инертностью.
Читать дальшеИнтервал:
Закладка:








