Николай Глинка - Общая химия
- Название:Общая химия
- Автор:
- Жанр:
- Издательство:неизвестно
- Год:неизвестен
- ISBN:нет данных
- Рейтинг:
- Избранное:Добавить в избранное
-
Отзывы:
-
Ваша оценка:
Николай Глинка - Общая химия краткое содержание
Учебное пособие предназначено для студентов нехимических специальностей высших учебных заведений. Оно может служить пособием для лиц, самостоятельно изучающих основы химии, и для учащихся химических техникумов и старших классов средней школы.
Легендарный учебник, переведенный на многие языки стран Европы, Азии, Африки и выпущенный общим тиражом свыше 5 миллионов экземпляров.
При изготовлении файла, использован сайт http://alnam.ru/book_chem.php
Общая химия - читать онлайн бесплатно ознакомительный отрывок
Интервал:
Закладка:
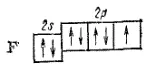
который и участвует в образовании ковалентной связи. Атом бериллия в невозбужденном состоянии (1s 22s 2) неспаренных электронов не имеет:
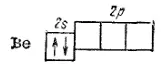
Поэтому для участия в образовании химических связей атом бериллия должен перейти в возбужденное состояние (1s 22s 12p 1):
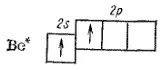
Образовавшийся возбужденный атом Be* обладает двумя неспаренными электронами: электронное облако одного из них соответствует состоянию 2s, другого — 2р. При перекрывании этих электронных облаков с р-электронными облаками двух атомов фтора могут образоваться ковалентные связи (рис. 38).
Однако, как уже было сказано, при затрате некоторой энергии вместо исходных s- и p-орбиталей атома бериллия могут образоваться две равноценные гибридные орбитали (sp-орбитали). Форма и расположение этих орбиталей показаны на рис. 39, из которого видно, что гибридные sp-орбитали вытянуты в противоположных направлениях.
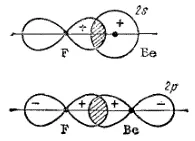
Рис 38. Схема перекрывания 2р-электронных облаков атомов фтора с 2s и 2р-электронными облаками атома бериллия (для каждой связи отдельно).
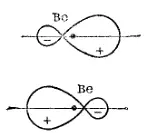
Рис. 39. Форма (схематическое изображение) и взаимное расположение гибридных sp-электронных облаков атома бериллия (для каждой гибридной орбитали отдельно).
- 131 -
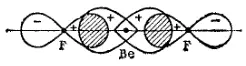
Рис. 40. Схема образования химических связей в молекуле BeF 2.
В целях упрощения рисунка гибридные sp-электронные облака атома бериллия изображены не полностью.
Перекрывание гибридных sp-электронных облаков атома бериллия с p-электронными облаками атомов фтора изображено на рис. 40. Благодаря вытянутой форме гибридных орбиталей достигается более полное перекрывание взаимодействующих электронных облаков, а значит, образуются более прочные химические связи. Энергия, выделяющаяся при образовании этих связей, больше, чем суммарные затраты энергии на возбуждение атома бериллия и гибридизацию его атомных орбиталей. Поэтому процесс образования молекулы BeF 2энергетически выгоден.
Рассмотренный случай гибридизации одной s- и одной р-орбитали, приводящий к образованию двух sp-орбиталей, называется sp-гибридизацией. Как показывает рис. 39, sp-орбитали ориентированы в противоположных направлениях, что приводит к линейному строению молекулы. Действительно, молекула BeF 2линейна, а обе связи Be-F в этой молекуле во всех отношениях равноценны.
Возможны и другие случаи гибридизации атомных орбиталей, однако число образующихся гибридных орбиталей всегда равно общему числу исходных атомных орбиталей, участвующих в гибридизации. Так, при гибридизации одной s- и двух р-орбиталей ( sp 2-гибридизация — читается «эс-пэ-два») образуются три равноценные sp 2-орбитали. В этом случае гибридные электронные облака располагаются в направлениях, лежащих в одной плоскости и ориентированных под углами 120° друг к другу (рис. 41). Очевидно, что этому типу гибридизации соответствует образование плоской треугольной молекулы.
Примером молекулы, в которой осуществляется sp 2-гибридизация, может служить молекула фторида бора BF 3. Здесь вместо исходных одной s- и двух р-орбиталей возбужденного атома бора
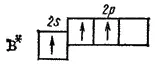
образуются три равноценные sp 2-орбитали. Поэтому молекула BF 3построена в форме правильного треугольника, в центре которого расположен атом бора, а в вершинах—атомы фтора. Все три связи B-F в молекуле BF 3равноценны.
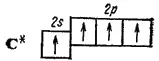
Если в гибридизации участвуют одна s- и три р-орбитали ( sp 3- гибридизация), то в результате образуются четыре гибридные sp 3-орбитали, вытянутые в направлениях к вершинам тетраэдра, т. е. ориентированные под углами 109°28' друг к другу (рис. 42). Такая гибридизация осуществляется, например, в возбужденном атоме углерода при образовании молекулы метана CH 4.
- 132 -
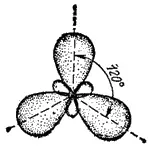
Рис. 41. Взаимное расположение гибридных sp 2-электронных облаков.
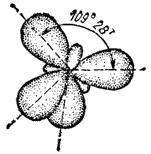
Рис. 42. Взаимное расположение гибридных sp 3-электронных облаков.
Поэтому молекула метана имеет форму тетраэдра, причем все четыре связи C-H в этой молекуле равноценны.
Вернемся к рассмотрению структуры молекулы воды. При ее образовании происходит sp 3-гибридизация атомных орбиталей кислорода. Именно поэтому валентный угол НОН в молекуле H 2O (104.5°) близок не к 90°, а к тетраэдрическому углу (109,5°). Небольшое отличие этого угла от 109,5° можно понять, если принять во внимание неравноценность состояния электронных облаков, окружающих атом кислорода в молекуле воды. В самом деле, в молекуле метана (I)

все восемь электронов, занимающие в атоме углерода гибридные sp 3-орбитали, участвуют в образовании ковалентных связей C-H. Это обусловливает симметричное распределение электронных облаков по отношению к ядру атома углерода. Между тем, в молекуле воды(II) только четыре из восьми электронов, занимающих гибридные sp 3-орбитали атома кислорода, образуют связи O-H, а две электронные пары остаются неподеленными, т. е. принадлежат только атому кислорода. Это приводит к некоторой асимметрии в распределении электронных облаков, окружающих атом кислорода, и, как следствие, к отклонению угла между связями O-H от 109,5°.
При образовании молекулы аммиака также происходит sp 3-гибридизация атомных орбиталей центрального атома (азота). Именно поэтому валентный угол HNH (107.3°) близок к тетраэдрическому. Небольшое отличие этого угла от 109,5° объясняется, как и в молекуле воды, асимметрией в распределении электронных облаков вокруг ядра атома азота: из четырех электронных пар три участвуют в образовании связей N — Н, а одна остается неподеленной.
Читать дальшеИнтервал:
Закладка:






